 06.09.2025
06.09.2025
Влияние коморбидного статуса на лечение пациента с поздней стадией ревматоидного артрита (клиническое наблюдение)
Ревматоидный артрит (РА) является самым распространенным и инвалидизирующим ревматическим заболеванием. Ведение больных РА является сложным диагностическим и лечебным процессом
Введение
Ревматоидный артрит (РА) – хроническое аутоиммунное заболевание соединительной ткани неизвестной этио-логии, в основе которого лежит иммуновоспалительный процесс, характеризующийся прогрессирующей эрозивной деструкцией суставов с поражением и нарушением функции внутренних органов [1, 2].
Причину развития заболевания связывают с генетической предрасположенностью в комплексе со средовыми факторами [1, 3, 4]. РА относится к наиболее распространенным аутоиммунным заболеваниям. Коэффициент поражения равен 0,5, что составляет 2% взрослого населения, соотношение женщин к мужчинам — 3:1 [1, 4]. Отсутствие своевременной диагностики и эффективной терапии может привести к утрате трудоспособности и инвалидизации пациента, что значительно влияет на качество его жизни [1, 5].
Патогенез РА заключается в антиген-специфической активации CD4+ Т-лимфоцитов, синтезирующих интерлейкин (ИЛ) 1 и 6, интерферон γ, а также в возникновении дисбаланса между гиперпродукцией провоспалительных и противовоспалительных цитокинов. Заболевание классифицируют по наличию ревматоидного фактора (РФ) и/или антител к циклическому цитруллинированному пептиду (АЦЦП) (серопозитивный, серонегативный), по клинической стадии (очень ранняя стадия, ранняя стадия, развернутая стадия, поздняя), по активности болезни (ремиссия, низкая, умеренная, высокая активность), по наличию внесуставных проявлений и по осложнениям [6, 7].
Клиническая картина складывается из суставных и внесуставных проявлений.
Заболевание, как правило, начинается постепенно и проявляется в виде утренней скованности не менее 1 ч и нарастающей артралгии, преимущественно в области мелких суставов кистей и стоп. В большинстве случаев поражение суставов симметричное и начинается с проксимальных межфаланговых (МФС), пястно-фаланговых суставов (ПФС), плюснефаланговых суставов (ПЛФС) или лучезапястных (ЛЗС) суставов. Суставные проявления можно разделить на 2 группы: потенциально обратимые, проявляющие в виде синовита, и необратимые структурные. Подобное разделение определяет прогноз заболевания после начала лечения [5, 8].
С течением времени у лиц, страдающих РА, могут формироваться различные деформации: «ревматоидная кисть», проявляющаяся в виде ульнарной девиации пястно-фаланговых суставов; поражение пальцев кистей по типу «бутоньерки» (сгибание в проксимальных МФС) или «шеи лебедя» (переразгибания в проксимальных МФС); деформация кисти по типу «пуговичной петли». Суставы стоп поражаются в области ПЛФС II–IV пальцев. Крупные суставы и позвоночник вовлекаются в патологический процесс значительно реже [9].
К внесуставным проявлениям относят: снижение массы тела на 10–20 кг в течение 6 мес., лихорадку во второй половине дня или вечером продолжительностью от 2 нед. до нескольких месяцев, периферическую лимфаденопатию, поражение мышц в виде миалгий, поражение кожи в виде капилляритов, геморрагического васкулита. Наблюдается возникновение ревматоидных узелков — безболезненных плотных образований округлой формы от 2 мм до 3 см в диаметре, локализующихся преимущественно подкожно на разгибательных поверхностях суставов. Поражение легких проявляется в виде диффузного интерстициального фиброза, плеврита, альвеолита, облитерирующего бронхиолита, поражение сердечно-соcудистой системы — в виде перикардита, коронарного артериита, атеросклероза, поражение почек — в виде гломерулонефрита, амилоидоза. Возможно также поражение глаз в виде иридоциклита, ирита, эписклерита. Наличие коморбидности у пациентов с РА существенно снижает благоприятный прогноз течения заболевания, качество жизни и определяет дальнейшую тактику ведения пациента [10–12].
Диагностика РА основывается на характерных клинических симптомах, диагностических и классификационных критериях, данных лабораторных и инструментальных исследований.
Диагностические критерии РА приняты Американской коллегией ревматологов (ACR) в 1987 г. [6]:
Утренняя скованность не менее 1 ч в течение 6 нед. и более.
Артриты трех и более суставных областей из 14 следующих: проксимальных МФС, ПФС, ЛЗС, локтевых, коленных, голеностопных суставов, ПЛФС в течение 6 нед. и более.
Артриты суставов кистей в течение 6 нед. и более.
Симметричный артрит.
Наличие ревматоидных узелков.
Выявление РФ в диагностических титрах.
Рентгенологические изменения, характерные для РА.
Ревматоидный артрит диагностируется минимум при четырех критериях из семи.
Для ранней диагностики РА разработаны классификационные критерии ACR/EULAR 2010 г.:
А. Клинические признаки поражения суставов (0–5 баллов).
В. Тесты на РФ и АЦЦП (0–3 балла).
С. Острофазовые показатели (0–1 балл).
D. Длительность синовита (0–1 балл).
Шесть и более баллов при исключении других причин артрита являются достаточными для постановки диагноза РА [6].
Лабораторно-инструментальная диагностика основывается на определении АЦЦП, РФ, острофазовых показателей в крови, проводится рентгенография кистей и стоп, магнитно-резонансная томография суставов при необходимости, ультразвуковое исследование суставов.
Лечение включает в себя немедикаментозную и медикаментозную терапию, а также ортопедическую и хирургическую коррекцию [13].
Немедикаментозная терапия состоит в коррекции образа жизни, отказе от курения, правильном питании, лечебной физкультуре, физиотерапии.
Медикаментозная терапия включает в себя ряд препаратов, направленных на патогенез заболевания.
I. Болезнь-модифицирующее лечение (направлено на разрешение воспаления и предотвращение рецидивов заболевания) [14]:
А. Синтетические болезнь-модифицирующие препараты:
1. Традиционные синтетические базисные противовоспалительные препараты (БПВП) (метотрексат, сульфасалазин, лефлуномид, плаквенил).
2. Ингибиторы янус-киназ (тофацитиниб, барицитиниб, упадацитиниб).
Б. Биологические БПВП:
1. Ингибиторы фактора некроза опухоли α (ФНО-α)и их рецепторов: инфликсимаб, голимумаб, адалимумаб, этанерцепт, цертолизумаба пэгол.
2. Анти-В-клеточные препараты (ритуксимаб).
3. Ингибиторы ко-стимуляции Т-лимфоцитов (абатацепт).
4. Ингибиторы интерлейкина 6 и их рецепторов (тоцилизумаб, сарилумаб, левилимаб, олокизумаб).
II. Противовоспалительная терапия: нестероидные противовоспалительные препараты (НПВП), глюкокортикостероиды (ГКС).
III. Ортопедическая и хирургическая коррекция состоит в применении ортезов, фиксирующих повязок и эндопротезировании суставов.
Таким образом, ведение больных с РА является сложным диагностическим и лечебным процессом. При курации таких пациентов необходимо учитывать не только тяжесть основного заболевания, но и наличие сопутствующей коморбидной патологии, которая может усложнять диагностический поиск, а также выбор таргетной терапии. Мы хотели бы представить клиническое наблюдение агрессивного течения заболевания у пациентки с РА с полиморбидными состояниями и продемонстрировать современные методы лечения данной патологии. Перед описанием клинического наблюдения у пациентки получено информированное согласие.
Клиническое наблюдение
Пациентка, 65 лет, пенсионерка, инвалид I группы по заболеванию «ревматоидный артрит», была госпитализирована в ревматологическое отделение клиники факультетской терапии ВМедА в июне 2022 г. с жалобами на боль, утреннюю скованность и ограничение движений в мелких суставах кистей и стоп, ЛЗС, локтевых, плечевых, коленных и тазобедренных суставах, общую слабость.
Из анамнеза известно, что заболевание дебютировало в 1999 г. с суставного синдрома воспалительного характера мелких суставов кистей и стоп. В 2001 г. перенесла туберкулез легких с исходом в излечение. С 2016 г. отмечала постепенное развитие контрактур верхних и нижних конечностей. По поводу данного заболевания ежегодно лечилась в профильных стационарах по месту жительства в г. Смоленске, где в 2021 г. диагностирован РА.
Рекомендованную терапию РА (метотрексат, преднизолон) до 2022 г. постоянно не получала в связи с развитием на фоне их приема выраженных диспепсических расстройств, повышения уровня трансаминаз, обострения герпетической инфекции. С 2022 г. отмечает ухудшение состояния в виде увеличения продолжительности утренней скованности, усиления болей, ограничения подвижности в суставах. Амбулаторно ревматологом возобновлена базисная терапия метотрексатом в дозе 15 мг/нед., на постоянный прием назначены НПВП и ГКС (преднизолон 10 мг/сут). В динамике, несмотря на проводимую терапию, состояние продолжало ухудшаться, нарастали болевой суставной синдром, утренняя скованность в пораженных суставах. Консультирована ревматологом кафедры факультетской терапии ВМедА, рекомендована госпитализация в специализированный ревматологический стационар с целью инициации генно-инженерной биологической терапии (ГИБТ).
В июне 2022 г. госпитализирована в клинику факультетской терапии. Основной диагноз: ревматоидный артрит, серопозитивный, АЦЦП-позитивный, поздняя клиническая стадия с системными проявлениями (гипотрофия мышц верхних и нижних конечностей, лимфаденопатия подмышечной, субпекторальной групп, ревматоидные узелки в области локтевых суставов и легких, пневмофиброз (множественные кисты в легких), миокардиодистрофия, похудание, нефропатия, анемия тяжелой степени), эрозивный, рентгенологическая стадия — IV, активность высокая (DAS28СРБ — 3,2). Функциональный класс III, дыхательная недостаточность I ст., хроническая сердечная недостаточность I ст., хроническая болезнь почек 3а ст.
Осложнения заболевания: вторичный полиостеоартроз с преимущественным поражением коленных, тазобедренных суставов, III–IV стадии, функциональная недостаточность сустава III.
Сопутствующие заболевания: посттуберкулезные изменения обоих легких (множественные очаговые уплотнения легочной ткани, субплевральные множественные воздушные кисты в S3, S5, S9, S10 правого легкого и в S5, S9, S10 левого легкого), левосторонний посттуберкулезный коксит. Дегенеративно-дистрофическое заболевание позвоночника. Остеохондроз шейного, грудного отдела позвоночника. Хронический бронхит, ремиссия. Киста левой почки. Двусторонняя нейросенсорная тугоухость.
На момент поступления в стационар состояние пациентки расценено как удовлетворительное, однако наблюдалось общее истощение, бледность кожных покровов, выраженная сгибательная контрактура суставов верхних и нижних конечностей (мелкие суставы кистей и стоп, локтевой, плечевой суставы, коленный, тазобедренный суставы), невозможность к самостоятельному передвижению (пациентка передвигалась в инвалидном кресле).
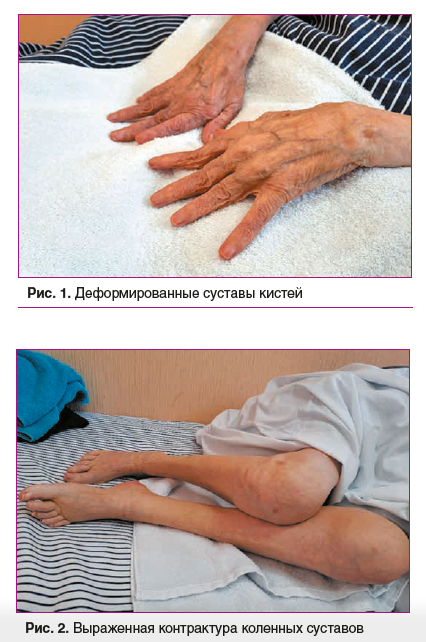
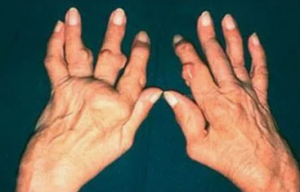
При объективном обследовании наблюдалась выраженная деформация суставов кистей (веретенообразные пальцы) (рис. 1), а также сгибательная контрактура обоих коленных суставов (рис. 2). Выявлены ревматоидные узелки в области локтевых суставов. При аускультации сердца на верхушке ослабление первого тона. Частота дыхательных движений — 14 в 1 минуту, при аускультации на фоне ослабленного дыхания выслушивалась крепитация в базальных отделах обоих легких.
Лабораторно в гемограмме выявлена анемия тяжелой степени (гемоглобин до 70 г/л), гематокрит до 20,9%, эритроциты 2,5×1012/л. Также выявлена высокая острофазовая и иммунологическая активность заболевания: СОЭ до 43 мм/ч, СРБ 35,41 мг/л, фибриноген 6,95 г/л, РФ 58,7 МЕ/мл, АЦЦП 155,7 ЕД/мл.
По данным КТ органов грудной клетки обнаружены множественные очаговые уплотнения легочной ткани и субплевральные множественные воздушные кисты в S3, S5, S9, S10 правого легкого и в S5, S9, S10 левого легкого. Данные изменения расценены как системное проявление основного заболевания в виде поражения легких (КТ-паттерн: обычная интерстициальная пневмония — «сотовое легкое»). Также выявлены признаки тяжелого системного остеопороза.
На рентгенограмме суставов кистей (рис. 3): справа и слева в прямой проекции — неравномерное сужение суставных щелей ПФС и МФС, остеопороз всех костей правой и левой кисти на всем протяжении, несоответствие суставных поверхностей костей (по типу «веретенообразных пальцев»), множественные эрозии и деформации суставных поверхностей пястных костей и фаланг пальцев.
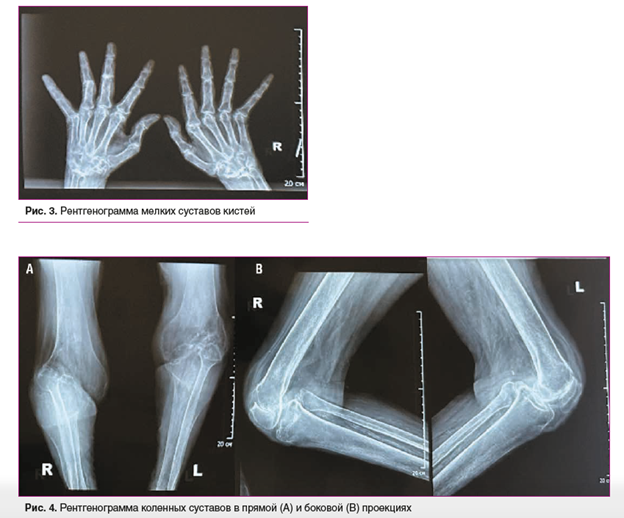
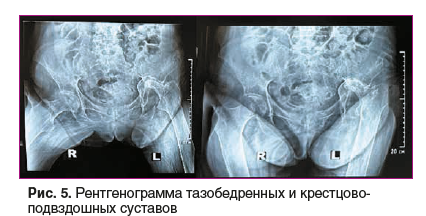
На рентгенограмме коленных суставов (рис. 4): справа и слева в прямой проекции — суставная щель не определяется, деформация латеральных надмыщелков бедренных костей и проксимального эпифиза большеберцовой кости, несоответствие суставных поверхностей сочленяющихся костей, наблюдается околосуставной остеопороз. На рентгенограмме тазобедренного сустава (рис. 5): слева — вколачивание и значительная деформация головки тазобедренной кости в кости таза, справа — сужение суставной щели, головка бедренной кости и вертлужная впадина с наличием эрозий, признаки остеопороза, крестцово-подвздошные суставы — признаки двустороннего сакроилиита.
В рамках алгоритма обследования пациентки перед инициацией ГИБТ проведен диаскин-тест (от 17.06.2022), выявлена гиперергическая реакция (папула 20 мм). Консультирована фтизиатром, рекомендован прием противотуберкулезных препаратов на 3 мес. Принято решение инициацию ГИБТ отложить. В клинике проводилось лечение (июнь 2022 г.): БПВП (метотрексат 15 мг/нед.), препараты железа (ферлатум 2 фл/сут), инициирована противотуберкулезная терапия: изониазид 0,6/сут, пиразинамид 1,5/сут. В связи с низкой эффективностью базисной терапии, наличием высокой острофазовой и иммунологической активности заболевания, системных проявлений болезни проведена пульс-терапия метилпреднизолоном 500 мг № 3. Пациентка выписана на амбулаторный этап лечения с рекомендациями продолжить прием БПВП и противотуберкулезную терапию.
В феврале 2023 г. повторно госпитализирована в клинику факультетской терапии с целью обследования, уточнения степени активности заболевания, уточнения характера сопутствующей патологии, инициации ГИБТ. В рамках алгоритма обследования перед инициацией ГИБТ выполнен диаскин-тест, с результатами повторно консультирована фтизиатром, противопоказаний к проведению ГИБТ не выявлено. Выполнена инициация ГИБТ в варианте блокатора CD20+ ритуксимаба 1000 мг в/в капельно с премедикацией метилпреднизолоном 250 мг в/в капельно. Выбор ритуксимаба был обусловлен наличием у пациентки высокой иммунологической активности заболевания, тяжелых системных проявлений болезни, высоким риском возникновения бактериальных инфекций, перенесенной туберкулезной инфекцией. По данным ряда зарубежных и отечественных исследований, риски реактивации данной инфекции отсутствуют у ритуксимаба по сравнению с препаратами класса ингибиторов ФНО-α [15–19]. Также с целью терапии тяжелого системного остеопороза выполнено введение антирезорбтивного препарата деносумаб 60 мг подкожно.
На фоне проводимой терапии пациентка отметила улучшение самочувствия в виде купирования утренней скованности и болевого суставного синдрома в пораженных суставах, уменьшения общей слабости. По данным лабораторных исследований (от 13.02.2023) достигнуто снижение острофазовых показателей (СОЭ 20 мм/ч, СРБ 6 г/л, фибриноген 4,8 г/л) и повышение уровня показателей «красной крови» (гемоглобин 99 г/л, эритроциты 3,3×1012/л). Выписана на амбулаторный этап лечения. Повторное введение ритуксимаба запланировано через 6 мес.
Обсуждение
Данный клинический случай демонстрирует сложности и особенности ведения больного с РА после перенесенной туберкулезной инфекции. Сложности лечебного процесса заключались в выборе препарата, а также поздней инициации адекватного лечения. При выборе ГИБП в лечении РА у нашей пациентки мы учитывали следующие аспекты: тяжелое течение РА, наличие коморбидных заболеваний, в частности перенесенной туберкулезной инфекции в анамнезе. В официальных клинических рекомендациях [1] ингибиторы ФНО-α не рекомендованы этой категории пациентов ввиду высокого риска реактивации туберкулезной инфекции. В этом случае препаратами первой линии являются ингибиторы CD20-рецепторов, а именно ритуксимаб. В нашем клиническом наблюдении правильный подбор ГИБТ сопровождался значимым положительным эффектом в виде снижения интенсивности суставного синдрома, острофазовой и иммунологической активности заболевания. Лечение не привело к ухудшению течения коморбидных состояний.
Выводы
Ранняя диагностика и своевременное начало терапии РА являются основополагающими факторами достижения ремиссии, благоприятного течения и прогноза заболевания, предотвращения поражения жизненно важных органов и систем, инвалидизации пациента.
Особенностью данного клинического наблюдения явилось агрессивное течение РА с быстрым развитием тяжелых деформаций периферических суставов и системных проявлений на фоне отсутствия адекватной базисной терапии РА.
Наличие коморбидной патологии, высокий риск развития инфекционных осложнений могут быть препятствием для проведения ГИБТ либо служить поводом для ее переноса на более поздние сроки.
Ритуксимаб у данной пациентки с РА является препаратом выбора ввиду наличия высокой иммунологической и острофазовой активности заболевания, риска реактивации туберкулезной инфекции.
Список литературы
1. Российские клинические рекомендации. Ревматология. Под ред. Насонова Е.Л. М.: ГЭОТАР-Медиа; 2017. [Russian clinical guidelines. Rheumatology. Nasonov E.L., ed. M.: GEOTAR-Media; 2017 (in Russ.)].
2. Smolen J.S., Aletaha D., McInnes I.B. Rheumatoid arthritis. Lancet. 2016;388(10055):2023–2038. DOI: 10.1016/S0140-6736(16)30173-8.
3. Насонов Е.Л. Ревматология. Под ред. Насонова Е.Л., Насоновой В.А. М.: ГЭОТАР-Медиа; 2010. [Nasonov E.L. Rheumatology. Nasonov E.L. Nasonova V.A., eds. M.: GEOTAR-Media; 2010 (in Russ.)].
4. Venetsanopoulou A.I., Alamanos Y., Voulgari P.V., Drosos A.A. Epidemiology of rheumatoid arthritis: genetic and environmental influences. Expert Rev Clin Immunol. 2022;18(9):923–931. DOI: 10.1080/1744666X.2022.2106970.
5. Cush J.J. Rheumatoid Arthritis: Early Diagnosis and Treatment. Rheum Dis Clin North Am. 2022;48(2):537–547. DOI: 10.1016/j.rdc.2022.02.010.
6. Мазуров В.И., Гайдукова И.З. Методические рекомендации. Ревматоидный артрит — основы диагностики и лечения. 2021:5–8. [Mazurov V.I., Gaidukova I.Z. Guidelines. Rheumatoid arthritis — the basics of diagnosis and treatment. 2021:5–8 (in Russ.)].
7. McInnes I.B., Schett G. The pathogenesis of rheumatoid arthritis. N Engl J Med. 2011;365(23):2205–2219. DOI: 10.1056/NEJMra1004965.
8. Lehmann J., Kyburz D. Rheumatoide Arthritis. Ther Umsch. 2023;80(1):27–33 (in German). DOI: 10.1024/0040-5930/a001403.
9. Ахунова Р.Р., Ахунова Г.Р. Суставной синдром в клинической практике. РМЖ. 2022;6:42–45. [Akhunova R.R., Akhunova G.R. Articular syndrome in clinical practice. RMJ. 2022;6:42–45 (in Russ.)].
10. Мурадянц А.А., Шостак Н.А. Ревматоидный артрит: клинические ситуации и алгоритмы лечения. РМЖ. 2016;2:89–95. [Muradyants A.A., Shostak N.A. Rheumatoid arthritis: clinical situations and treatment algorithms. RMJ. 2016;2:89–95 (in Russ.)].
11. Князева Л.И., Князева Л.А., Горяйнов И.И. Внутренние болезни. Учебник для студентов мед. вузов. 4-е изд., перераб. и доп. Курск; 2013. [Knyazeva L.I., Knyazeva L.A., Goryainov I.I. Internal illnesses. Textbook for medical students. 4th ed., revised. Kursk; 2013 (in Russ.)].
12. Maharaj A.B., Daikh D.I. Diagnosing rheumatoid arthritis: challenges and opportunities. Best Pract Res Clin Rheumatol. 2022;36(1):101743. DOI: 10.1016/j.berh.2022.101743.
13. Каратеев Д.Е., Лучихина Е.Л. Современная стратегия терапии ревматоидного артрита. РМЖ. 2012;20(30):1504–1509. [Karateev D.E., Luchikhina E.L. Modern strategy for the treatment of rheumatoid arthritis. RMJ. 2012;20(30):1504–1509 (in Russ.)].
14. Кольцова Е.Н., Лукина Г.В., Шмидт Е.И. и др. Анализ нежелательных явлений при использовании генно-инженерных биологических и таргетных синтетических базисных противовоспалительных препаратов у пациентов с ревматоидным артритом. РМЖ. 2022;6:30–35. [Koltsova E.N., Lukina G.V., Shmidt E.I. et al. Analysis of adverse events when using genetically engineered biological and targeted synthetic basic anti-inflammatory drugs in patients with rheumatoid arthritis. RMJ. 2022;6:30–35 (in Russ.)].
15. Насонов Е.Л. Эффективность и безопасность ингибиторов фактора некроза опухоли-α при ревматоидном артрите. РМЖ. 2008;24:1602. [Nasonov E.L. Efficacy and safety of tumor necrosis factor-a inhibitors in rheumatoid arthritis. RMJ. 2008;24:1602 (in Russ.)].
16. Каратеев Д.Е. Ритуксимаб в современной терапии ревматоидного артрита Фарматека. 2010;5:26–32. [Karateev D.E. Rituximab in modern therapy of rheumatoid arthritis Farmateka. 2010;5:26–32 (in Russ.)].
17. Tavakolpour S., Alesaeidi S., Darvishi M. et al. A comprehensive review of rituximab therapy in rheumatoid arthritis patients. Clin Rheumatol. 2019;38(11):2977–2994. DOI: 10.1007/s10067-019-04699-8.
18. Lopez-Olivo M.A., Amezaga Urruela M., McGahan L. et al. Rituximab for rheumatoid arthritis. Cochrane Database Syst Rev. 2015;1:CD007356. DOI: 10.1002/14651858.CD007356.pub2.
19. Головизнин М.В., Тимофеев В.Т., Лахонина Н.С., Булдакова Ю.Р. Иммунологические исследования в ревматологической клинике. Путь длиной в семь десятилетий. РМЖ. 2018;12(II):92–98. [Goloviznin M.V., Timofeev V.T., Lakhonina N.S., Buldakova Yu.R. Immunological studies in a rheumatology clinic. A journey of seven decades. RMJ. 2018;12(II):92–98 (in Russ.)].
Авторы:
Свинцицкая И.С., Елбаев Р.Ж., Нуршакирова И.Е. , Жигулина А.И.
Военно-медицинская академия, Санкт-Петербург, Россия
Юдин В.А., Свинцицкая И.С.
Войсковая часть 53594, Уссурийск
Теги: ревматоидный артрит
234567 Начало активности (дата): 06.09.2025
234567 Кем создан (ID): 989
234567 Ключевые слова: ревматоидный артрит, иммуновоспалительный процесс, ревматоидная кисть, антитела, серопозитивный, ритуксимаб, туберкулез
12354567899
Похожие статьи
Среднесрочные результаты хирургического лечения пациентов с посттравматическим артрофиброзом локтевого суставаРентген на дому 8 495 22 555 6 8
Микробиологический фактор при остеоартритах
Стенозирующий лигаментит пальцев кисти
Первичное и ревизионное эндопротезирование тазобедренного сустава с восполнением дефектов вертлужной впадины



