 23.02.2026
23.02.2026
Роль мультиспиральной компьютерной томографии в оценке резектабельности опухоли при раннем раке гортани: клинический случай
По результатам обследования пациента в едином диагностическом алгоритме, оценки течения опухолевого процесса по данным МСКТ при совместной деятельности лучевого диагноста и врача-хирурга был выбран вариант оперативного лечения методом эндоларингеальной резекции (ЭЛР).
Введение.
В градации по частоте встречаемости злокачественными новообразованиями среди ЛОРорганов рак гортани стоит на первом месте, составляя 5–7% от всех злокачественных новообразований. В 2021 году в России было зарегистрировано 6189 новых пациентов с диагнозом рака гортани, подавляющее большинство составили мужчины (96,0%), что вероятнее всего объясняется широкой распространенностью курения среди представителей сильного пола [1].
Согласно классификации TNM (Tumor, Nodus, Metastasis) рак гортани подразделяют на 4 стадии. Первая и вторая стадии относятся к раннему раку гортани. Стадия Т1 определяется в случае, когда опухоль ограничивается одним анатомическим элементом гортани, не доходя до его границы, при этом подвижность голосовых складок сохранена.
Стадия T2 — опухоль полностью занимает один анатомический элемент и доходит до его границы, при этом голосовые складки ограниченно подвижны [2].
Одним из методов лечения при раннем раке гортани выступает эндоларингеальная резекция.
Отбирая пациентов для хирургического лечения, врач должен быть уверен в возможности радикального оперативного вмешательства, так как это является одним из основных факторов, определяющих успешные онкологические результаты [3].
Метод МСКТ позволяет получить наиболее функциональные данные о распространенности опухоли и сохранности голосовых складок [4]. В сравнении с МРТ и ПЭТ-КТ мультиспиральная компьютерная томография остается наиболее доступным для пациентов и быстрым вариантом диагностики, при этом демонстрируя высокие показатели информативности и точности результатов исследования [5]. Несмотря на то, что МСКТ входит в стандарт при диагностике рака гортани всех стадий, остаются нерешенные аспекты в рамках более детальной диагностики при раннем раке гортани.
В 2020 г. Европейским обществом отоларингологов был создан контрольный список для предоперационной оценки опухолей гортани, подлежащих лечению с помощью трансоральной микрохирургии [6]. Предложенный контрольный список визуализации представляет собой руководство для хирургов, выполняющих такого рода вмешательства.
Однако данная работа дает приблизительное представление, не демонстрируя вычислительные показатели для оценки резектабельности опухоли методом мультиспиральной компьютерной томографии.
Основанием для нашего исследования послужило отсутствие в отечественных работах и недостаточная разработанность зарубежных исследований по изучению возможностей применения МСКТ с целью оценки резектабельности раннего рака гортани для проведения эндоларингеальной резекции. В представленном клиническом случае отражены данные МСКТ и важные критерии для оценки резектабельности опухоли при раннем раке гортани, а именно, расстояние от опухоли до передней комиссуры, задней комиссуры и щитовидного хряща (околоскладочное пространство), а также разработанная нами форма оценки резектабельности опухоли, заполняемая врачом лучевым диагностом для дальнейшей передачи врачухирургу с целью оптимизации процесса и более точной диагностики опухолевого процесса.
Клинический случай.
Пациент Ц., мужчина, 68 лет. Курит в течение 55 лет по 2 пачки в день. Впервые жалобы на осиплость голоса появились в сентябре 2024 г., лечение не проводилось, в феврале 2025 г. обратился за медицинской помощью к ЛОР-врачу в поликлинику по месту жительства. Пациент был осмотрен ЛОР-врачом с подозрением на злокачественное образование. Был направлен в ГБУЗ ООД.
Во время проведения локального осмотра в полости рта, глотки без особенностей, слизистая оболочка бледно-розового цвета. При непрямой ларингоскопии гортань подвижная, на левой голосовой складке определяется бугристая опухоль, розового цвета, вестибулярные складки без признаков опухолевого роста. Регионарные лимфатические узлы не пальпируются.
Согласно данным ФЛС, гортань симметричная, подвижная. Левая голосовая складка разрушена по всему протяжению, в ее проекции мелкозернистая ткань, кровоточивая при биопсии, признаков роста опухоли на вестибулярную складку нет. В подскладочном отделе гортани и верхней трети трахеи — без признаков опухолевой инфильтрации. Правая голосовая складка в средней трети с белесоватым утолщением слизистой оболочки 2×3 мм, гиперкератоз. Во время исследования взята биопсия: биопсия № 1 и цитология № 1 — с левой голосовой складки; биопсия № 2 и цитология № 2 — с правой голосовой складки.
Результаты.
№ 1 — биопсийный материал из патологического очага на поверхности левой голосовой складке. Представлен фрагментами опухоли с морфологической картиной плоскоклеточной карциномы без ороговения. Под № 2 — в биоптатах слизистой оболочки правой голосовой складке признаки хронического ларингита. В дистрофически измененном покровном плоском эпителии фокусы гиперкератоза и пролиферации клеток базального слоя.
Пациент был госпитализирован в ГБУЗ ООД в марте 2025 года с диагнозом: рак гортани, 1 стадия T1N0M0 2 кл.гр. По данным общего анализа крови, общего анализа мочи показатели соответствуют возрастной норме.
Согласно заключению рентгенографического исследования грудной клетки патологических изменений нет. Заключение УЗИ лимфатических узлов шеи: патологически измененных лимфатических узлов не выявлено. По результатам УЗИ органов брюшной полости: диффузные изменения поджелудочной железы. Признаков вторичного поражения органов опухолевым процессом отмечено не было. МСКТ проводилось с внутривенным болюсным контрастированием. Для контрастирования использовался препарат Ниоскан 350.
Согласно инструкции, расчет дозы в миллилитрах на килограмм массы тела не предусмотрен. Для взрослого пациента рекомендуется вводить 100–150 мл препарата. В связи с этим мы применяли Ниоскан 350 в дозировке 100 мл для данного пациента. По данным мультиспиральной компьютерной томографии шеи: на левой голосовой складке определяется объемное образование смешанного типа роста, занимающее всю длину голосовой складки, прилежит к морганиевому желудочку (закрыт), вестибулярная складка без признаков роста (рис. 1, 2)
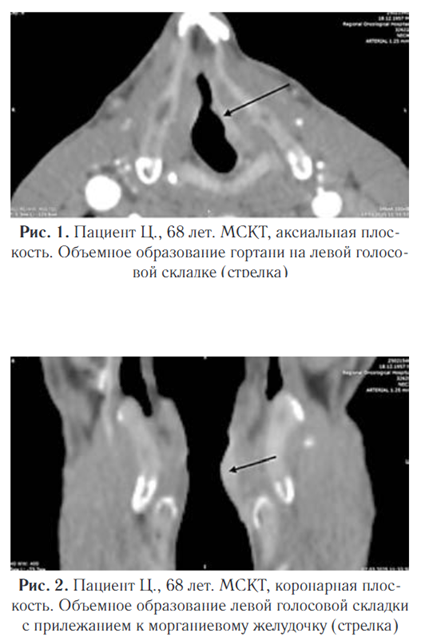
Плотность новообразования в нативную фазу исследования составила 47 HU, в артериальную фазу отмечено равномерное накопление контрастного вещества до 111 HU, в венозную фазу вымывание контрастного вещества — 102 HU. Особое внимание уделялось визуализации степени инфильтрации опухоли в морганиев желудочек и вестибулярную складку, что позволяло объективно оценить степень вовлеченности окружающих тканей и прогнозировать дальнейшее течение патологического процесса. Размеры образования: в аксиальной плоскости 18,5 мм (длина), 4,1 мм (ширина), в коронарной плоскости 17,8 мм (вертикаль) (рис. 3, 4).
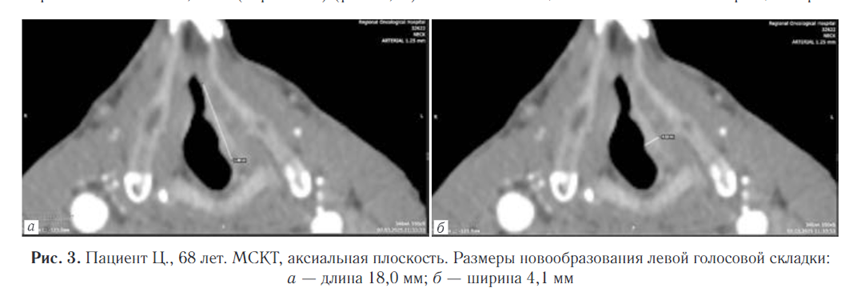
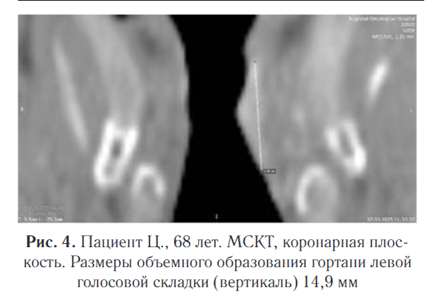
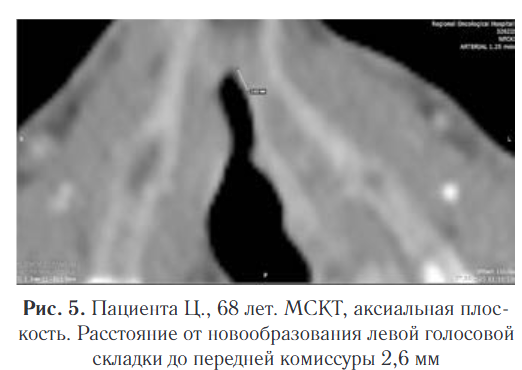
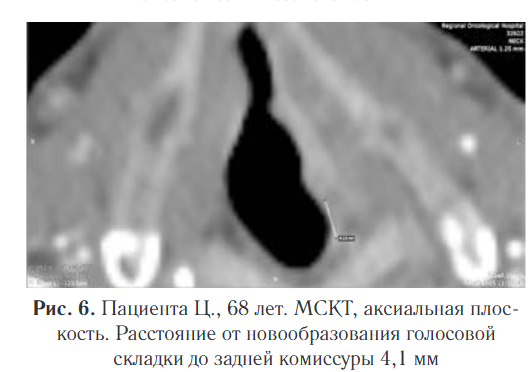
Проводилась оценка параметров инфильтрации тканей в аксиальной плоскости. Внимание уделялось измерению расстояний до передней и задней комиссур, имеющему значение в варианте возможного распространения опухолевого процесса на соседние голосовые складки. В этой анатомической области мягкие ткани характеризуются минимальной толщиной по отношению к хрящам гортани, что могло быстро привести к инвазии патологического процесса. Расстояние от новообразования до передней комиссуры у пациента составляло 2,6 мм, до задней комиссуры — 4,1 мм (рис. 5, 6).
Околоскладочное пространство выступает важной анатомической частью гортани, поскольку из него рак может беспрепятственно прорастать в околоскладочную область без выраженных клинических проявлений.
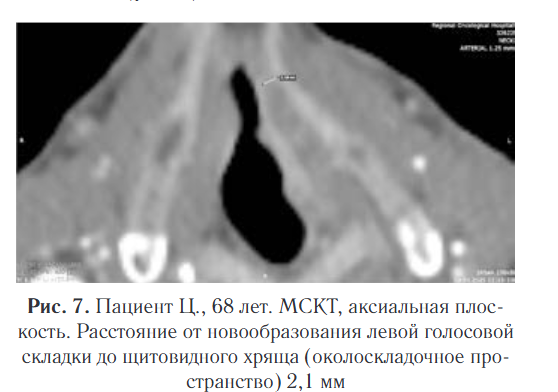
Околоскладочное пространство в представленном случае было свободно на расстоянии 2,1 мм (рис. 7).
Остальные параметры согласно МСКТ соответствовали норме. Прилежащие мягкотканные структуры лица не изменены, сохранены, плотность обычная. Нами была разработана форма для оценки злокачественного процесса при раннем раке гортани складочного отдела для определения резектабельности опухоли по данным МСКТ (табл. 1).
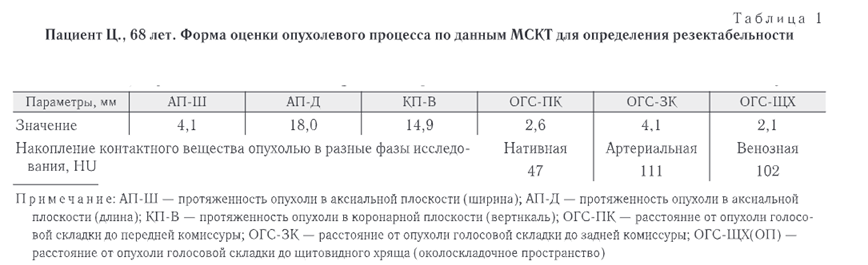
Все данные пациента были отражены в данной форме. Согласно полученным данным обследования, опухоль была определена как резектабельная ввиду отсутствия инвазии в щитовидный хрящ, перстневидный хрящ гортани и зоны передней комиссуры. Расстояние от новообразования до передней и задней комиссур, свободное от патологического очага, позволяло осуществить эндоларингэктомическое удаление опухоли с минимальным риском осложнений, равно как и отсутствие поражения злокачественной тканью прилегающих тканей околоскладочного пространства. Пациенту было выполнено хирургическое вмешательство методом ЭЛР.
Операционный материал после маркировки был направлен в патогистологическое отделение для итоговой оценки. Через 7 дней был предоставлен результат гистологического заключения: «Левая голосовая складка с опухолью»: слизистая размером 1,5×1×0,5 см, поверхность шероховатая. При гистологическом исследовании на протяжении 0,6 см обнаружен рост плоскоклеточной карциномы без ороговения с инвазией в строму на глубину 0,2 см (1–4). «Левая вестибулярная складка с морганиевым желудочком (границы резекции)»: фрагмент ткани размером 2,5×1,5×0,5 см.
При микроскопии без признаков опухолевого роста (5–9) (рис. 8).
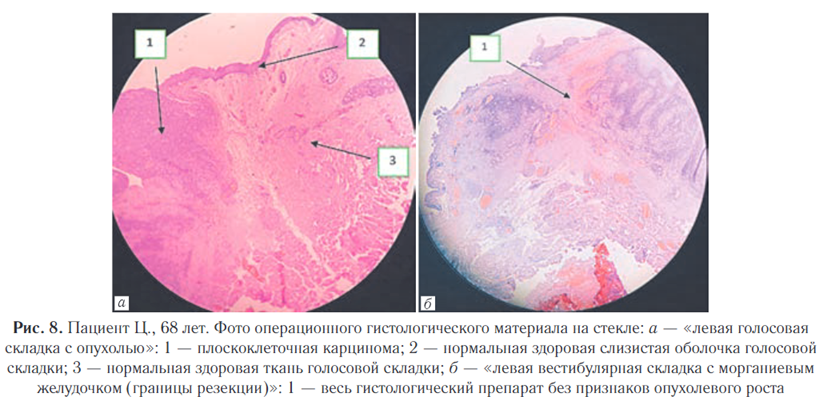
Заключение
Инвазивная плоскоклеточная карцинома гортани слева без ороговения.
Итоговый диагноз: рак гортани 1 стадия T1N0M0 2 кл.гр.
Пациенту рекомендовано наблюдение у онколога, ЛОР-врача по месту жительства. Повторная явка в ГБУЗ «Областной онкологический диспансер» на контрольный осмотр через 3 месяца.
Таким образом, были представлены данные о состоянии окружающих мягких тканей гортани вблизи соседних анатомических структур, а также об отсутствии инвазии патологического процесса в околоскладочное пространство. Макроскопический и микроскопический анализ удаленного материала продемонстрировал успешность выбранного плана лечения, демонстрируя отрицательный край резекции, что выступает «золотым стандартом» подтверждения радикальности оперативного вмешательства
Обсуждение.
Представленный клинический случай отражает важность точной диагностики раннего рака складочного отдела гортани при оценке резектабельности опухоли. Как отмечают J-P. Machiels и соавт. (2020), предоперационная оценка перед трансоральными микрохирургическими вмешательствами, такими как лазерная резекция, основывается на тщательном картировании с использованием визуализационных методов. Эти процедуры включают систематическую эндоскопическую и радиологическую оценку степени поражения, что напрямую влияет на планирование и выполнение операции, а также на ее конечный результат [7].
Анализ литературы показывает, что за последние 10 лет при диагностике резектабельности опухоли в случае рака гортани Т1, Т2 наибольший акцент как на неблагоприятной области делается на поражении передней комиссуры. Вовлечение передней является одним из факторов, способствующих рецидиву, и связано с более низким уровнем локального контроля, сохранением гортани и выживаемостью при данном заболевании [8].
При этом область задней комиссуры и околоскладочное пространство остается менее значимой областью. По нашему мнению, важно учитывать все области, потенциально неблагоприятные для проведения ЭЛР.
Если опухоль возникает в задней части голосовых связок, она может распространиться на черпаловидный хрящ и заднюю комиссуру. Чем ближе опухоль расположена к задней комиссуре, тем выше риск поражения черпаловидного хряща, а поражение данного хряща повышает риски стеноза гортани и трахеотомии [9]. Именно в связи с этим A. Sahul и соавт. (2023) в своей работе по визуализации рака гортани отмечают важность проведения КТ шеи в венозную фазу, чтобы контрастное вещество успело достичь нормальных и патологических мягких тканей, при этом сканирование проводится при спокойном дыхании пациента, чтобы можно былолучше оценить состояние передней и задней комиссуры при отведении голосовых связок [10].
В рамках формы оценки опухоли мы также отмечаем плотность опухоли в разные фазы исследования, чтобы врач-хирург при предварительной визуализации опухоли понимал, какие изображения КТ стоит наиболее детально рассмотреть перед операцией.
Согласно данным Европейского ларингологического общества, а также исследованиям S. Hans с соавт. (2022), эффективность проведения ЭЛР во многом зависит от опыта хирурга.
В отличие от открытых операций при ЭЛР младший хирург имеет больший обзор, чем более опытный специалист, а визуализацию опухоли зачастую сложно адекватно оценить непосредственно через ларингоскоп во время операции [11]. Именно поэтому подобные формы МСКТ во многом полезны для начинающих специалистов, имеющих меньший опыт проведения подобных операций, в качестве данных для разметки по результатам МСКТ.
В 2025 г. на выборке из 45 пациентов с ранним раком гортани, проходивших лечение на базе отделения хирургических методов лечения опухолей головы и шеи ГБУЗ ООД и подписавших информационное согласие на участие в исследовании, участники были разделены на две группы. В 1-ю группу вошли пациенты с первой стадией рака складочного отдела гортани — 25 (54,5%) больных, во 2-ю — пациенты со второй стадией рака складочного отдела гортани —20 (44,5%) человек. Выполнялась оценка опухолипо параметрам резектабельности, и после установлен по данным МСКТ, что области передней, задней комиссуры и околоскладочное пространство свободны от опухоли, проводилась операция методом эндоларингеальной резекции.
Результаты МСКТ сопоставлялись с данными гистологического заключения посредством программы IBM SPSS Statistics 23.
Корреляция МСКТ и результата гистологии (отрицательный край резекции) в соответствии с данными непараметрического критерия корреляции Спирмена составила r=0,4 — умеренная положительная связь (при p>0,01 — высокая значимость).
Кроме того, нами были получены минимальные значения расстояний до передней комиссуры, задней комиссуры и щитовидного хряща по данным МСКТ,которые рассматриваются как референтные в рамках нашего исследования, подобные варианты не рассчитывались в других исследованиях. Данные статистической обработки представлены в табл. 2.
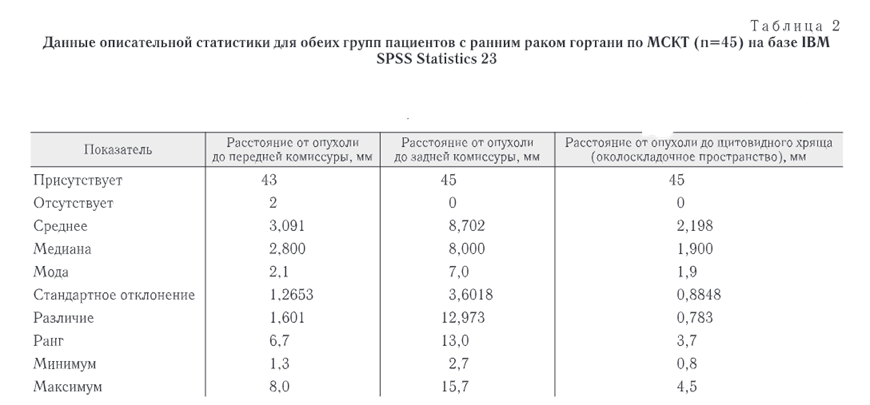
Таким образом, минимальные значения для обеих групп пациентов с ранним раком гортани по данным мультиспиральной компьютерной томографии составили 1,3 мм от опухоли до передней комиссуры, 2,7 мм — до задней комиссуры и 0,8 мм до щитовидного хряща (околоскладочное пространство). Данные расстояния выступили в качестве референтных, поскольку в рамках проведенного исследования отрицательный край резекции был получен в 93,4% случаев, только в одном (2,2%) наблюдении были получены артификационные изменения (которые отнесены к ложноотрицательному результату).
Несмотря на то, что успешность лечения и 5-летняя выживаемость при раннем раке гортани показывает высокие результаты, недостаточная диагностика и оценка может приводить к рецидивам и дальнейшему лечению пациента. В работе 2023 года А. В. Карпенко и соавт. приводят анализ результатов применения эндоларингеальной резекции, показывая, что, несмотря на то, что данный вариант лечения выступает основным при Т1, Т2 стадиях рака гортани, процент рецидивов при этом остается достаточно высоким (10,5% при отсутствии вовлечения передней комиссуры и 24,5% при ее вовлечении в опухолевый процесс), при том что с точки зрения потенциального прогноза лечение на начальных стадиях должно приводить к максимально эффективным вариантам выздоровления больных [12].
Важным фактором успеха проведения малоинвазивных операций выступает полная и точная визуализация процесса, обеспечившая предварительную оценку границ опухолевого процесса. Согласно исследованию F. Agnello и соавт. (2017), помимо выявления плоскоклеточной карциномы, врачу-рентгенологу важно установить степень ее распространения на подслизистые слои, хрящи гортани и окологортанные мягкие ткани, потому что наличие такого поражения затрудняет проведение консервативного хирургического лечения и лучевого воздействия [13].
Когда мы говорим о критериях резектабельности, необходимо отметить, что на сегодняшний момент нет единой схемы, при которой идет оценка области поражения опухолью. В работе S. L. van Egmond и соавт. (2018), посвященной метаанализу работ по эндоларингеальной резекции, точные критерии, единые для всех, не указываются, заметны вариации в выбираемых параметрах, операция проводится в большей степени на усмотрение хирурга и опыт организации, в которой проходит лечение пациент [14].
Представленный нами клинический случай предлагает обобщенный вариант визуализации процесса для более детального подхода к лечению раннего рака гортани складочного отдела. Подобные примеры помогают совершенствовать знания практикующих специалистов и могут способствовать повышению общего уровня оказания помощи пациентам с представленной патологией.
Цель нашего исследования согласуется с данными мировых тенденций, а именно рекомендациями Европейского ларингологического общества (2020), клиническими рекомендациями EHNS- ESMO-ESTRO (2020), рекомендациями по визуализации рака гортани и гортаноглотки (Индия, 2023), согласно которым делается акцент на создании мульти-модальных команд, предполагающих в том числе тесное сотрудничество визуальных диагностов и врачей- хирургов, что способствует повышению качества оказываемой медицинской помощи [6, 7, 15].
Заключение.
Для определения резектабельности опухолевого процесса в гортани перед проведением хирургического лечения в виде эндоларингеальной резекции необходима детальная оценка состояния опухоли и ее распространенности по данным МСКТ.
В случае обследования и предоперационной подготовки врач-рентгенолог и хирург, по нашему мнению, должны тесно взаимодействовать друг с другом для обсуждения различных случаев распространения опухоли, с целью сохранения значимых для пациента функций, снижения травматичности проводимого лечения и уменьшения рисков дальнейших рецидивов.
Сведения об авторах:
Демичев Эдуард Дмитриевич — врач-рентгенолог отделения лучевой диагностики МСКТ, врач — челюстно-лицевой хирург, врач-онколог онкологического отделения хирургических методов лечения опухолей головы и шеи государственного бюджетного учреждения здравоохранения «Областной онкологический диспансер»; 664035, г. Иркутск, ул. Фрунзе, д. 32
Селивёрстов Павел Владимирович — доктор медицинских наук, ведущий научный сотрудник, заведующий лабораторией лучевой диагностики научно-клинического отдела нейрохирургии федерального государственного бюджетного научного учреждения «Иркутский научный центр хирургии и травматологии»; 664003, г. Иркутск, ул. Борцов Революции, д. 1
Расулов Родион Исмагилович — доктор медицинских наук, профессор, заведующий кафедрой онкологии Иркутской государственной медицинской академии последипломного образования (ИГМАПО) — филиала федерального государственного бюджетного образовательного учреждения дополнительного профессионального образования «Российская медицинская академия непрерывного профессионального образования» Министерства здравоохранения Российской Федерации, заместитель главного врача по хирургической помощи государственного бюджетного учреждения здравоохранения «Областной онкологический диспансер»; 664035, г. Иркутск, ул. Фрунзе, д. 3
Теги: мультиспиральная компьютерная томография
234567 Начало активности (дата): 23.02.2026
234567 Кем создан (ID): 989
234567 Ключевые слова: мультиспиральная компьютерная томография, ранний рак гортани, эндоларингеальная резекция, клинический случай
12354567899
Похожие статьи
Мультиспиральная компьютерная томография (МСКТ)в оценке качества кости у больных врожденным ложным суставом голениМультиспиральная компьютерная томография как эффективный метод диагностики стенозов гортани и трахеи
Рентген на дому 8 495 22 555 6 8
Мультиспиральная компьютерная томография в диагностике травматического остеомиелита челюстно-лицевой области
Мультиспиральная компьютерная томография (МСКТ)в оценке качества кости у больных врожденным ложным суставом голени



