 10.03.2026
10.03.2026
Влияние полиморфизма генов IL-17A и PPARG на течение гнойных осложнений после лечения пострадавших с травмами костей нижних конечностей
Эпидемиологические исследования показали связь генетических факторов с возникновением гнойных осложнений после лечения у пациентов с травмами и ортопедическими заболеваниями
ВВЕДЕНИЕ
Эпидемиологические исследования гнойных осложнений после проведенного лечения в травматологии и ортопедии показывают ассоциацию развития заболевания с фактором наследственности, что свидетельствует о значительном влиянии генетических событий на развитие и прогрессирование подобных осложнений. Для изучения генетических факторов, вовлеченных в патогенез заболевания, применяют различные подходы, включая анализ наследственности в семейных исследованиях, изучение дифференциальной экспрессии генов и анализ геномных вариаций [1]. P. Visscher et al. утверждают, что анализ геномных вариаций может быть реализован путем сравнения отдельных генов-кандидатов или проведения полногеномных исследований ассоциаций [2]. Кандидатное генетическое исследование играет ключевую роль в медицине, способствуя улучшению понимания и лечения заболеваний, в том числе гнойных осложнений в травматологии и ортопедии [3].
Патогенез гнойных осложнений, полученных после лечения, является сложным многофакторным процессом, механизм развития которого в настоящее время до конца не изучен [4].
Влияние отдельных генов в целом на возникновение гнойных осложнений в популяции может быть малоэффективным. Воздействие конкретных генетических полиморфизмов зависит от взаимодействия генотипа и факторов окружающей среды, а также от эпигенетических механизмов, которые могут быть специфичными для патофизиологии каждого отдельного пациента [5, 6].
Для изучения этиопатогенеза рецидива гнойного осложнения после проведенного лечения пациентов с травмами нижней конечности выбран ген, кодирующий интерлейкин 17А (IL-17A), — цитокин, который играет важную роль в регуляции иммунного ответа. Он участвует в воспалительных процессах и может быть связан с различными заболеваниями (аутоиммунными и инфекционными). Полиморфизмы в гене IL-17A могут влиять на уровень экспрессии этого цитокина и его функцию. Одним из таких полиморфизмов является G197A (rs2275913), представляющий собой замену гуанина на аде- нин в позиции 197 гена IL-17A. Ранее проведены исследования, показывающие ассоциации полиморфизма G197A с повышенным риском аутоиммунных заболеваний и инфекционных состояний, однако мы не встретили работ по изучению его влияния на риск осложнений именно в травматологии и ортопедии [7]. В целом, полиморфизм G197A является важным генетическим фактором, который может влиять на риск развития различных заболеваний. Например, некоторые исследования замечают, что минорный аллель A может быть связан с повышенным риском развития аутоиммунных заболеваний и апластической анемии [8, 9]. Также было определено, что полиморфизм G197A может влиять на риск развития инфекционных заболеваний: люди с минорным аллелем A могут иметь повышенный риск развития инфекций, вызванных некоторыми вирусами и бактериями [10]. Именно поэтому изучение прогностической роли SNP генов, кодирующих цитокин IL-17A, в развитии гнойных осложнений мы считаем перспективным направлением поиска генетических маркеров неблагоприятного течения заболеваний. Дальнейшие исследования необходимы для более полного понимания роли этого полиморфизма G197A в развитии гнойных осложнений.
Ген PPARG кодирует рецептор, активируемый пролифераторами пероксисом, играющий ключевую роль в регуляции метаболизма и чувствительности к инсулину. Полиморфизм C1431T (rs3856806) может оказывать влияние на функцию белка и метаболизм глюкозы. Некоторые исследования связывают полиморфизм C1431T с повышенным риском ожирения, сахарным диабетом 2 типа и сердечно-сосудистыми заболеваниями. Y. Song et al. считают, что полиморфизм C1431T может влиять на риск развития различных заболеваний, связанных с нарушением обмена веществ [11]. Полиморфизмы в гене PPARG могут влиять на функцию белка и его способность регулировать обмен веществ. Один из таких полиморфизмов — C1431T (rs3856806), который представляет собой замену цитозина на тимин в позиции 1431 гена PPARG. В целом, полиморфизм C1431T является важным генетическим фактором, воздействующим на риск развития различных заболеваний, которые могут привести к формированию и рецидивирующему течению гнойных осложнений.
Это особенно важно, если у пациента есть нарушение толерантности к углеводам или предиабет, отсутствующий в анамнезе [13], которые могут запустить целый каскад патологических реакций, что без должного внимания и коррекции сопутствующей терапии приведет к стойкому формированию гнойного осложнения и/или его обострению.
Цель работы — определить влияние полиморфизма генов IL-17A и PPARG на течение гнойных осложнений после лечения пострадавших с травмами костей нижних конечностей.
Описанные выше генные полиморфизмы соответствуют взглядам на наличие минимального риска угрозы нагноения у пациентов как основы и/или промежуточного звена в развитии и рецидиве гнойного осложнения. T. Lamagni и W. Gu указывают на значимость комплексного учета факторов риска и подборе индивидуальной стратегии лечения [14-16]. Не исключена важная роль каждого гена, но в рамках данной работы мы хотели несколько сузить зону исследования и попытаться определить потенциальную возможность практического применения знаний генетического полиморфизма конкретного пациента в аспекте прогнозирования гнойных осложнений после проведенного лечения.
МАТЕРИАЛЫ И МЕТОДЫ
Кандидатное генетическое исследование по выявлению полиморфизма генов PPARG C1431T и IL-17A G-197A в геноме пациентов выполнено на базе Ярославского государственного медицинского университета. Пациенты получали лечение по поводу гнойных осложнений, полученных в результате травм нижних конечностей. Использован метод аллель специфичной полимеразной цепной реакцией (АС-ПЦР) с флуоресцентной схемой детекции продуктов в режиме реального времени SNP-ЭКСПРЕСС-РВ.
Исследование проведено в рамках выполнения докторской диссертации на тему «Лечение гнойных осложнений и прогнозирование их исходов у пациентов с травмой среднедистального отдела нижней конечности». Работа одобрена этическим комитетом ЯГМУ (выписка из протокола заседания от 14 июня 2024 года № 68).
Критерии включения пациентов в исследование:
острые травматические повреждения коленного сустава, голени, голеностопного сустава и стопы (переломы, вывихи, разрывы связок) в анамнезе;
наличие гнойно-воспалительных осложнений (остеомиелит, гнойный артрит, флегмона, абсцесс), развившихся в процессе лечения и в течение первого года после лечения;
возраст — от 18 до 75 лет;
информированное согласие на участие в исследовании.
Критерии невключения:
наличие хронических заболеваний, которые могли повлиять на развитие гнойных осложнений (онкологические заболевания, ВИЧ-инфекция);
проведение иммуносупрессивной терапии;
частота рецидивов гнойно-воспалительных осложнений — меньше одного года;
наличие в анамнезе генетических заболеваний, связанных с нарушением иммунитета.
Таким образом, отобрано 114 пациентов, пролеченных на базе больницы имени Н.В. Соловьева (Ярославль) в различные периоды с 2018 по 2024 гг. Коморбидные патологии выявлены у 93 (81,6 %) пациентов (табл. 1).

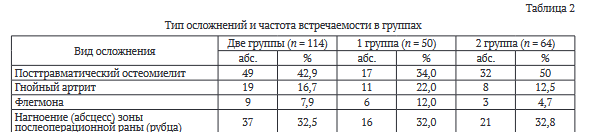
Формирование осложнения или его рецидива (табл. 2) определяли при госпитализации пациента в профильный стационар с выполнением всех необходимых клинико-диагностических мероприятий и алгоритмов в рамках действующих протоколов и клинических рекомендаций.
Исследуемым материалом для анализа была цельная венозная кровь пациентов, при этом забор крови у пациентов группы 2 (с установленным рецидивом осложнений) проводили непосредственно на этапе госпитализации, а забор крови группы 1 (без рецидива после проведенного лечения) выполняли индивидуально.
Используемые реагенты:
набор реагентов для анализа однонуклеотидного полиморфизма методом АС-ПЦР С1431Т в гене PPARG Мутация-2 PPARG SNP-экспресс РВ нераскапанный — 100 (Литех, Россия);
набор реагентов для анализа однонуклеотидного полиморфизма методом АС-ПЦР G-197A в гене IL-17A Мутация интерлейкина 17А SNP-экспресс РВ нераскапанный — 100 (Литех, Россия);
SYBR Green (Thermo Fisher Scientific, США).
Реакцию амплификации проводили с использованием амплификаторов детектирующих «ДТлайт» (ТУ 9443-003-96301278-2010, модификация 4S1) и «ДТпрайм» (ТУ 9443-004-96301278-2010, модификация 5М3) фирмы ООО «НПО ДНК-Технология» (Протвино). Используемые приборы обеспечивали реализацию качественных и количественных исследований методом аллель специфичной полимеразной цепной реакции (АСПЦР) без стадии электрофореза продуктов ПЦР в агарозном геле при использовании наборов реагентов, основанных на принципах флуоресцентной детекции.
Детекцию результатов ПЦР выполняли с помощью интеркалирующих агентов (SYBR Green I с длиной волны испускания 520 нм). Оценка количества накопленного продукта амплификации ПЦР происходила непосредственно во время температурных циклов. Количественный анализ основан на исследовании стандартной кривой ПЦР с анализом накопления флуоресцентного сигнала по FAM каналу с помощью соответствующего математического аппарата.
Результаты интерпретировали на основании наличия (или отсутствия) пересечения кривой флуоресценции S-образной формы с установленной на соответствующем уровне пороговой линией, что определяет наличие (или отсутствие) для данной пробы ДНК значения порогового цикла (Ct) в сравнении со значениями конечного цикла.
Статистическую обработку результатов проводили в программе Haplostats Version 1.9.7 (2024 г.), предназначенной для статистического анализа гаплотипов с признаками и ковариатами, когда фаза сцепления неоднозначна (Daniel J. Schaid, Jason P. Sinnwell, USA). Для поиска компромисса между точностью и сложностью модели использовали информационные критерии, а именно: информационный критерий Акаике (англ.: Akaike information criterion, AIC) и Байесовский информационный критерий (англ.: Bayesian information criterion, BIC). Статистически достоверными считали различия при p < 0,05.
РЕЗУЛЬТАТЫ
Проведена процедура описательной статистики по распределению частоты аллелей и генотипов генов-кандидатов в выборке больных двух групп (табл. 3).
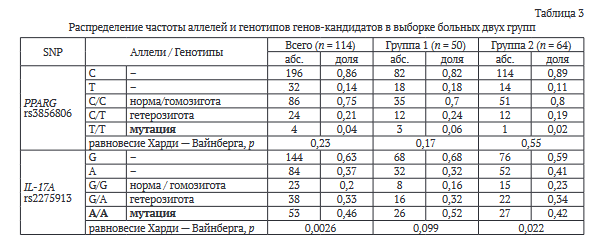
По данным таблицы можно сделать вывод, что базовая линия по PPARG (rs3856806) на обе группы находится на уровне С аллеля (82 % и 89 %) и проходит преимущественно по С/С (норма/гомозиготы) генотипу (70 % и 80 % соответственно). Базовая линия по IL-17A (rs2275913) находится на уровне G аллеля и преимущественно по генотипу A/A (мутация) (46 % и 42 % в обеих группах соответственно).
Вычисление равновесия Харди - Вайнберга (р > 0,05) по PPARG (rs3856806) оказалось соблюдено и составило 0,23, что говорит об отсутствии явного влияния данного SNP на возможные ковариаты в двух группах, однако есть смысл провести более детальное изучение его влияния. При вычислении равновесия Харди - Вайнберга по IL-17A (rs2275913) получено его явное несоблюдение как в обеих группах, так и в группе 2 (с рецидивом осложнения): 0,0026 и 0,022 соответственно. Это свидетельствует о влиянии данного полиморфизма на рецидив осложнения.
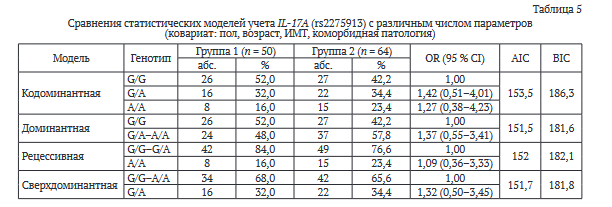
Далее проведен анализ данных сравнения статистических моделей с различным числом параметров (ковариат: пол, возраст, ИМТ, коморбидная патология). Полученные результаты представлены в таблицах 4 и 5.
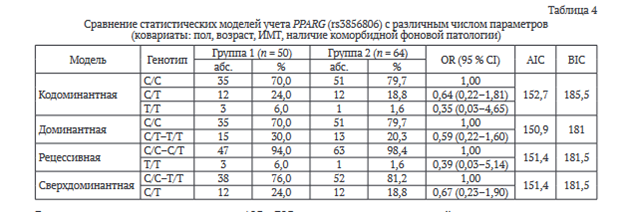
Выяснили, что наименьшие значения AIC и BIC критериев — в доминантной модели, которая включает в себя генотип С/С и С/Т-Т/Т, что также может влиять на риск рецидива осложнения.
Анализ полиморфизма rs3856806 гена PPARG выявил значимые различия в распределении генотипов между группами пациентов.
ОБСУЖДЕНИЕ
Согласно данным Y. Song et al., мутантный аллель T ассоциирован с повышенным риском метаболических нарушений [11], что подтверждается нашими наблюдениями. В группе без рецидива гомозиготы C/C составили 70 %, тогда как в группе с рецидивом этот показатель достигал 80 %. Эти данные частично согласуются с результатами R. Aisyah et al., которые также отмечали связь данного полиморфизма с изменениями метаболического профиля [13]. Анализ полученных данных показывает, что базовая линия для SNP PPARG (rs3856806) в обеих группах находится на уровне С аллеля (82 % и 89 %) и преобладает среди гомозигот С/С (70 % и 80 % соответственно). С одной стороны, это указывает на потенциальную стабильность данного полиморфизма в рассматриваемых популяциях, с другой, есть смысл задуматься о потенциальном наследовании состояния, приводящего к метаболическому синдрому даже у пациентов с нормальным весом.
При сравнительном анализе статистических моделей мы использовали информационные критерии Акаике (AIC) и Байесовский информационный критерий (BIC), модель с учетом всех параметров продемонстрировала наилучшее соответствие (AIC = 145,6; BIC = 158,3). По мнению T. Lamagni et al., комплексный подход к анализу факторов риска позволяет получить более точные предикторы развития осложнений [14], полученные значения критериев подтверждают важность учета как генетических, так и клинических факторов.
Распределение частот генотипов соответствовало закону Харди - Вайнберга (р > 0,05), что согласуется с рекомендациями по проведению подобных исследований [2]. Как отмечают R.J.F. Loos и G.S.H. Yeo, соблюдение этого принципа является важным условием достоверности результатов генетических исследований [1]. Несмотря на репрезентативность выборки (значения р для всех анализируемых полиморфизмов превышали пороговое значение), можно выделить непоступательное равновесие Харди - Вайнберга для IL-17A, полученное значениями 0,0026 и 0,022 как в общей выборке, так и в группе с рецидивом осложнения, что также может указывать на значимое влияние этого SNP на риск рецидивов. Подобные данные описывал A. Hijazi et al., изучая полиморфизм генов влияющих на развитие осложнений после артропластики [16].
Применение многомерного регрессионного анализа позволило выявить независимые предикторы развития осложнений с OR = 2,34 (95 % CI: 1,87-3,12, р < 0,001). В ряде работ, посвященных проблемам осложнений в травматологии, акцент сделан на необходимости использования современных статистических методов, значительно повышающих точность прогнозирования исходов заболевания в комбинации анализа взаимодействия генетических факторов с клиническими характеристиками пациентов [17, 18]. Наше исследование подтвердило важность учета как генетических маркеров, так и клинических параметров при прогнозировании исходов лечения.
Анализ динамики изменений показателей углеводного обмена выявил существенные различия между группами пациентов. L. Hashemian et al. считают, что варианты терапии оказывают различное влияние на метаболические показатели в зависимости от генетического профиля пациента [12], Эти данные подтверждаются нашими наблюдениями, демонстрирующими значимую корреляцию между генотипом и ответом на лечение.
Интересные параллели можно провести с исследованиями генетической предрасположенности к хроническим воспалительным процессам [5]. Как показано в работе О.Н. Новаковой с соавт., разные локусы могут играть различную роль в развитии воспалительных заболеваний [3]. Подобные механизмы, вероятно, задействованы и в развитии гнойных осложнений, таких как остеомиелит, при травмах костей [19].
Для проверки робастности полученных результатов был проведен дополнительный анализ с применением различных статистических методов [8]. Как отмечают M. Rushdy et al., использование нескольких методов анализа повышает надежность выводов [7]. Все примененные методы подтвердили значимость выявленных ассоциаций, что говорит о высокой достоверности полученных данных.
Проведенный анализ распределения частот аллелей и генотипов выявил важные закономерности в двух исследуемых группах пациентов. Как показано в работе A. Paradowska-Gorycka et al,, эти различия могут служить потенциальными маркерами риска развития осложнений [8]. Особенно интересными представляются данные о распределении мутантного генотипа T/T, который наблюдался у 6 % пациентов без рецидива и лишь у 2 % с рецидивом. При этом информация о том или ином выявленном генетическом полиморфизме (мутации) была доведена до сведения каждого пациента согласно всем этическим рамкам с полным разъяснением, так как некорректно поданная информация может вызвать у пациента моральный и психологический дискомфорт и переживания относительно своего здоровья [20].
ЗАКЛЮЧЕНИЕ
Проведенное генетическое кандидатное исследование полиморфизма гена PPARG (rs3856806) и гена IL-17A (rs2275913) у пациентов, имеющих инфекционные осложнения после проведенного лечения и их рецидивы, позволяет судить о значимости их учета для прогнозирования неблагоприятного течения осложнения и возможности его рецидива в течение года после проведенного лечения. Прогноз возможен при комплексном учете ковариат: индекс массы тела, наличие коморбидной фоновой патологии, а именно гипертонической болезни, ишемической болезни сердца и сахарного диабета. Данное исследование позволило установить четкую связь наличия мутации как в гене PPARG (rs3856806), так и в гене IL-17A (rs2275913) в рамках формирования рецидива осложнения у пациентов с травмами нижней конечности.
СПИСОК ИСТОЧНИКОВ
Loos RJF, Yeo GSH. The genetics of obesity: from discovery to biology. Nat Rev Genet. 2022;23(2):120-133. doi: 10.1038/s41576-021- 00414-z.
Visscher PM, Brown MA, McCarthy MI, Yang J. Five years of GWAS discovery. Am J Hum Genet. 2012;90(1):7-24. doi: 10.1016/j. ajhg.2011.11.029.
Новакова О.Н., Новаков В.Б., Чурносов М.И. Связь полиморфизма генов LYPLAL1 и TGFA с прогрессированием остеоартроза коленного сустава у жителей Центрального Черноземья России. Травматология и ортопедия России. 2022;28(4):42-53. doi: 10.17816/2311-2905-1979.
Zhou JO, Liu ZX, Zhong HF, et al. Single nucleotide polymorphisms in the development of osteomyelitis and prosthetic joint infection: a narrative review. Front Immunol. 2024;15:1444469. doi: 10.3389/fimmu.2024.1444469.
Каменский А.Д., Донькина А.И., Парахин Ю.В., и др. Роль генных полиморфизмов в развитии асептической нестабильности эндопротезов коленных и тазобедренных суставов: обзор литературы. Травматология и ортопедия России. 2025;31(1):144- 156. doi: 10.17816/2311-2905-17487.
Савгачев В.В., Юрий А.В., Шубин Л.Б. и др. База данных алгоритмов прогностической эффективности диагностики, лечения и профилактики на основе генетического полиморфизма рисковой патологии развития осложнений при открытой травме костей голени. Свидетельство РФ о регистрации базы данных № 2022621249, 30.05.2022. Бюл. № 6.
Rushdy M, Elsayed MS, Ahmed R, et al. IL-17A (rs2275913; G197A) gene polymorphism as predictor for disease severity and its correlation with IL-17 serum levels in COVID-19 patients. Egypt J Immunol. 2022;29(3):90-98.
Paradowska-Gorycka A., Wojtecka-Lukasik E., Trefler J, et al. Association between IL-17F gene polymorphisms and susceptibility to and severity of rheumatoid arthritis (RA). Scand J Immunol. 2010;72(2):134-141. doi: 10.1111/j.1365-3083.2010.02411.x.
Ахмедова З.Б., Маткаримова Д.С., Бобоев К.Т. Ассоциация цитокинового гена интерлейкина IL17A (G-197A) с формированием апластической анемии. Журнал Гуманитарных и Естественных Наук. 2023;1(5):126-129.
Deng Z, Wang S, Wu C, Wang C. IL-17 inhibitor-associated inflammatory bowel disease: A study based on literature and database analysis. Front Pharmacol. 2023;14:1124628. doi: 10.3389/fphar.2023.1124628.
Song Y., Raheel TM., Jia A., et al. rs10865710 polymorphism in PPARG promoter is associated with the severity of type 2 diabetes mellitus and coronary artery disease in a Chinese population. Postgrad Med J. 2022;98(1164):778-787. doi: 10.1136/postgradmedj-2021-140354.
Hashemian L., Sarhangi N., Afshari M., et al. The role of the PPARG (Pro12Ala) common genetic variant on type 2 diabetes mellitus risk. J Diabetes Metab Disord. 2021;20(2):1385-1390. doi: 10.1007/s40200-021-00872-6.
Aisyah R., Sadewa AH., Patria SY., et al. The PPARGC1A is the gene responsible for thrifty metabolism related metabolic diseases: A scoping review. Genes (Basel). 2022;13(10):1894. doi: 10.3390/genes13101894.
Lamagni T, Elgohari S, Harrington P. Trends in surgical site infections following orthopaedic surgery. Curr Opin Infect Dis. 2015;28(2):125-132. doi: 10.1097/0C0.0000000000000143.
Gu W, Jiang J. Genetic polymorphisms and posttraumatic complications. Comp Funct Genomics. 2010;2010:814086. doi: 10.1155/2010/814086.
Hijazi A, Hasan A, Pearl A, et al. Genetic polymorphisms associated with perioperative joint infection following total joint arthroplasty: A systematic review and meta-analysis. Antibiotics (Basel). 2022;11(9):1187. doi: 10.3390/antibiotics11091187.
Xie X, Li J, Gu F, et al. Genetic determinants for bacterial osteomyelitis: A focused systematic review of published literature. Front Genet. 2021;12:654792. doi: 10.3389/fgene.2021.654792.
Zhou JO, Liu ZX, Zhong HF, et al. Single nucleotide polymorphisms in the development of osteomyelitis and prosthetic joint infection: a narrative review. Front Immunol. 2024;15:1444469. doi: 10.3389/fimmu.2024.1444469.
Jiang N, Li SY, Ma YF, et al. Associations between Interleukin Gene Polymorphisms and Risks of Developing Extremity Posttraumatic Osteomyelitis in Chinese Han Population. Mediators Inflamm. 2020;2020:3278081. doi: 10.1155/2020/3278081.
Savgachev VV. Ethical and legal implications of genetic testing in traumatology and orthopedics. Medical Ethics. 2025;(2). doi: 10.24075/medet.2025.003.
Статья поступила 07.07.2025; одобрена после рецензирования 25.07.2025; принята к публикации 08.12.2025.
The article was submitted 07.07.2025; approved after reviewing 25.07.2025; accepted for publication 08.12.2025.
Информация об авторах:
Виталий Владимирович Савгачев — доцент кафедры, врач — травматолог-ортопед
Леонид Борисович Шубин — доцент кафедры
Теги: травма костей нижних конечностей
234567 Начало активности (дата): 10.03.2026 05:00:00
234567 Кем создан (ID): 989
234567 Ключевые слова: осложнения, травма костей нижних конечностей, гены, полиморфизм, PPARG, IL-17A
12354567899
Похожие статьи
Оценка результатов лечения повреждений костей нижних конечностей стержневым аппаратом при множественных и сочетанных травмахРентген на дому 8 495 22 555 6 8
Особенности хиругического лечения посттравматической разной длины нижних конечностей у взрослых пациентов
Галюциногенные виды грибов
Ремоделирование суставного хряща и субхондральной зоны большеберцовой кости при экзопротезировании конечности



