 27.04.2026
27.04.2026
Результаты дифференцированного подхода к открытой декомпрессии срединного нерва при синдроме запястного канала
Открытая декомпрессия срединного нерва — наиболее частая операция, выполняемая при синдроме запястного канала (СЗК).
ВВЕДЕНИЕ
Синдром запястного канала (СЗК) — это мононейропатия срединного нерва, обусловленная его компрессией окружающими тканями. Распространённость СЗК составляет 150-276 человек на 100 тыс. населения. Течение — прогрессирующее, резистентное к консервативной терапии, склонное к реци- дивированию, что предопределяет необходимость оперативного лечения, являющегося эффективным в 70-90 % клинических наблюдений [1].
Одна из клинических форм СЗК — идиопатическая, без явных причин (острой травмы, посттравматических деформаций кисти и лучезапястного сустава, эндокринных, метаболических или хронических системных заболеваний, внутриневральных опухолей). Считается, что заболеванию способствуют многократная нагрузка на кисть при сгибании в запястье, длительное ее нахождение в одном положении, игра на вибрирующих инструментах. Высокий риск развития заболевания имеют монтажники, упаковщики, сборщики, художники, ювелиры, делопроизводители, пианисты [1].
Открытая декомпрессия срединного нерва — наиболее частая операция при СЗК, позволяющая в короткие сроки не только купировать изматывающую боль и усилить чувствительность на пальцах кисти, но и достигнуть стойкого клинического улучшения. Однако рассечение поперечной связки запястья (ПСЗ) оказывает негативное влияние на биомеханику кисти и является предпосылкой для возникновения нежелательных состояний, таких как снижение силы захвата кисти и появление «опорной боли» (англ.: pillar pain) [2, 3, 4, 5, 6].
Для профилактики неблагоприятных последствий рассечения ПСЗ кистевыми хирургами предложен ряд способов ее восстановления [7, 4]. При этом авторы принимали во внимание то обстоятельство, что ПСЗ является не только передней границей запястного канала, но и местом прикрепления мышц тенара и гипотенара [3].
Известно, что примерно половину площади передней поверхности связки с лучевой стороны занимают мышцы возвышения большого пальца (m. flexor pollicis brevis, abductor pollicis brevis) [8]. Кроме того, в 55 % клинических наблюдений эти мышцы прикрепляются на локтевой стороне, в проекции места предполагаемого рассечения связки [9]. В таких ситуациях мышцы либо пересекают, либо отслаивают в лучевую сторону, что позволяет рассечь ПЗК в локтевой части запястного канала, избежав повреждения срединного нерва и его моторной ветви, и проведя при этом их полноценную ревизию [10].
Отрицательным последствием такого вмешательства является то, что после отслоения или пересечения мышцы тенара теряют точку прикрепления, что в последующем вызывает их гипо- или атрофию и неблагоприятно сказывается на восстановлении функции кисти в целом [11].
Цель работы — провести сравнительный анализ ближайших и отдаленных результатов оперативного лечения пациентов с СЗК после открытой декомпрессии в трех вариантах: без восстановления ПСЗ, с рефиксацией мышц тенара и с пластикой ПСЗ.
С целью профилактики подобных осложнений мы разработали способ рефиксации мышц возвышения большого пальца после открытой декомпрессии запястного канала [12].
МАТЕРИАЛ И МЕТОДЫ
Объект исследования — 80 пациентов с идиопатическим СЗК, которым с 01.01.2024 по 01.06.2025 выполнили открытую декомпрессию срединного нерва: 67 женщин и 13 мужчин среднего возраста 58 лет (36-86 лет). У 12 человек операции провели на обеих кистях с интервалом не менее трех месяцев. Операцию на одной кисти считали одним клиническим наблюдением. Всего выполнили 92 хирургических вмешательства. Операции на правой кисти провели в 61 (66 %), а на левой — в 31 (34 %) клиническом наблюдении.
Характеристика работы — нерандомизированное, проспективное, одноцентровое, продольное, контролируемое в параллельных группах клиническое исследование. Критерий включения — диагностированный до операции и подтвержденный в ее ходе СЗК. Критерии невключения — наличие у пациентов сопутствующих системных, метаболических и эндокринных заболеваний, последствий перелома костей кисти и предплечья, синдрома кубитального канала, рецидива СЗК. Никто из пациентов из исследования исключен не был.
Первичная конечная точка исследования — оценка эффективности оперативного лечения пациентов с СЗК путем открытой декомпрессии срединного нерва с рефиксацией мышц возвышения большого пальца и открытой декомпрессии срединного нерва с реконструкцией поперечной связки запястья, а также выработка рекомендаций по дифференцированному оперативному лечению в зависимости от анатомических особенностей запястья и паталогических изменений, выявленных в этой области.
Вторичные конечные точки исследования — анализ клинических показателей (силовой захват кисти, повседневная активность, тяжесть симптомов и функциональных нарушений), ЭНМГ-показателей (амплитуда М-ответа короткой мышцы, отводящей большой палец, дистальная латентность моторных волокон срединного нерва, скорость проведения импульса по моторным волокнам срединного нерва, скорость проведения импульса по сенсорным волокнам срединного нерва).
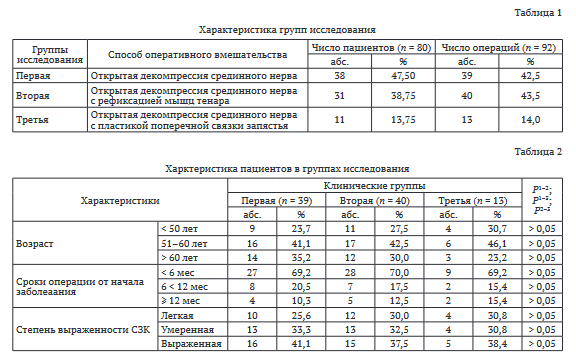
В зависимости от способа оперативного вмешательства все клинические наблюдения разделили на три группы (табл. 1). В первую группу вошли 38 пациентов (39 операций), которым после декомпрессии срединного нерва ПСЗ не восстанавливали. Вторая группа включала 31 пациента (40 операций), у которых мышцы возвышения большого пальца кисти (m. flexor pollicis brevis и m.abductor pollicis brevis) перекрывали линию предполагаемого рассечения ПСЗ. Место прикрепления мышц аккуратно отсепаровывали с подлежащей поверхностной частью связки и после декомпрессии запястного канала производили их рефиксацию, не прибегая к пластике ПЗК. Эту операцию осуществляли в соответствии с разработанным нами способом [11]. Третью группу составили 11 пациентов (13 операций), которым после декомпрессии срединного нерва производили пластику ПСЗ в соответствии с иным, ранее предложенным также нами способом [13].
Клинические группы (табл. 2) являлись сопоставимыми по возрасту, срокам выполнения операции от начала заболевания, степени выраженности СЗК, которую определяли в соотвеетствии с классификацией J. Beck [14].
При постановке диагноза СЗК учитывали жалобы пациентов на боль в кисти, преимущественно в ночные и утренние часы, чувство онемения в зоне иннервации срединным нервом, длительность заболевания и безуспешность консервативного лечения, наличие положительных клинических симптомов Фалена, Тинеля, теста «стряхивания кисти» (англ.: flick maneuver), «теста на царапины» (англ.: scratch collapse test), а также результаты ЭНМГ и УЗИ.
Показаниями к операции считали установленный кистевым хирургом диагноз СЗК, подтвержденный данными ЭНМГ и УЗИ, отсутствие клинического улучшения после консервативного лечения как минимум в течение трех месяцев, отрицательную динамику ЭНМГ-показателей.
Выбор способа оперативного лечения осуществляли, с одной стороны, опираясь на данные предоперационного инструментального ообследования (ЭНМГ, УЗИ), а с другой — основываясь на сведениях, полученных в ходе интраоперационной визуализации патологических изменений в области операции. Окончательное решение о способе операции принимали непосредственно в ходе хирургического вмешательства.
Так, если интраоперационно выявляли выраженный теносиновит сгибателей, препятствующий полноценному восстановлению ПСЗ, то предпочтение отдавали изолированной декопрессии срединного нерва без пластики ПЗК (первая группа). Если при УЗИ запястного канала или интраоперационно обнаруживали, что в месте предполагаемого рассечения ПСЗ находятся мышцы тенара, то их отсепа- ровывали вместе с поверхностной частью подлежащей связки, а после ее рассечения единым блоком рефиксировали (вторая группа). Если пациентами являлись люди, профессиональная деятельность которых была связана с постоянными движениями кисти под нагрузкой, то выполняли открытую декомпрессию запястного канала с истинной пластикой ПЗК (третья группа).
Эффективность хирургического лечения оценивали по восьми критериям, из них четыре являлись клиническими (величины силового захвата кисти, повседневной активности, тяжести клинических симптомов и функционального дефицита) и четыре — электронейромиографическими (амплитуда М-ответа короткой мышцы, отводящей большой палец, дистальная латентность моторных волокон срединного нерва, скорость проведения импульса по моторным и сенсорным волокнам срединного нерва). Все эти показатели изучили в динамике: перед операцией, через три и шесть месяцев после операции.
Величину силового захвата кисти определяли с использованием ручного пружинного динамометра ДК-50 (ЗАО «Нижнетагильский медико-инструментальный завод», Россия). Исследование на каждой руке проводили дважды с интервалом в одну минуту, после чего вычисляли средний показатель.
Выраженность повседневной активности пациентов определяли по опроснику DASH [15, 16, 18].
Для оценки результатов лечения применяли опросник BCTO [17, 18, 19].
Функциональный статус периферических моторных и сенсорных волокон срединного нерва изучали на обеих руках, используя стандартные программы электромиографа Лайтбокс (Нейрософт, Россия), два кабеля подключения одноразовых электродов с коннектором типа «аллигатор», «защищенным от прикосновения» (англ.: touch-proof), черного и красного цвета, заземляющий электрод, одноразовый накожный электрод 22 х 34 мм. Обследование выполняли по стандартным методикам [20].
Ультразвуковое исследование проводили на обеих верхних конечностях с помощью аппарата Samsung Medison HS 40, используя линейный датчик с частотой 3-16 МГц. В ходе сканирования идентифицировали срединный нерв, его размеры, структуру, места сдавления нерва на запястье и в верхней трети предплечья, расположение мышц тенара в зоне запястного канала, состояние окружающих тканей, мышц и сухожилий.
Статистический анализ данных выполняли в среде SPSS 25 (IBM SPSS Statistics, США, лицензия № 5725-А54). Соответствие величин количественных признаков нормальному закону распределения проверяли с помощью критерия Шапиро - Уилка и Колмогорова - Смирнова, с поправкой Лилифорса. Описательную статистику представляли в виде среднего и стандартного отклонения (M ± SD). Сравнение групп осуществляли с помощью рангового дисперсионного анализа Краскела - Уоллиса, критериев Манна - Уитни, парного критерия Вилкоксона, х2 Пирсона (для номинальных признаков).
Для визуализации полученных данных использовали графики типа «усатый ящик» (англ.: boxplot), отражающие медиану, квартили, минимум и максимум. Критическое значение уровня значимости принимали равным 0,05 во всех случаях, кроме межгрупповых сравнений в дисперсионном анализе, где применяли поправку Бонферрони с критическим значением р = 0,017.
Хирургическая техника
Общие, одинаковые для всех условия операции, характер хирургического доступа и этапы операции у пациентов первой группы соответствовал принципам, отраженным нами ранее [19].
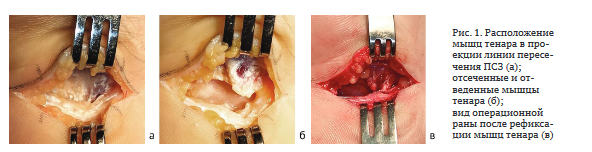
У пациентов второй группы производили аналогичный первой группе разрез кожи и апоневроза. ПСЗ рассекали по ее локтевой стороне. Продвигаясь проксимально до места пересечения с мышцами тенара (рис. 1, а), разрезом, огибающим вершину прикрепления мышц, отсекали поверхностный листок связки вместе с мышцами. Отводили их кнаружи. Затем полностью рассекали поперечную связку запястья, а также глубокую фасцию предплечья (рис. 1, б). Ревизировали срединный нерв. Отсеченные мышцы вместе с участком связки рефиксировали (подшивали на прежнее место или кнаружи до 3 мм), используя П-образный шов с двумя блокирующими петлями с каждой стороны (рис. 1, в). После этого тремя-четырьмя отдельными швами сшивали ладонный апоневроз, что позволяло сместить мышцы тенара кнутри, уменьшив напряжение на точке их фиксации. На кожу накладывали швы по Донати.
У пациентов третьей группы разрезы кожи и апоневроза были такими же, как в первой и второй группах. ПСЗ рассекали, формируя два трапециевидных лоскута: лучевой (проксимальный) и локтевой (дистальный). После ревизии, мобилизации и эпиневротомии срединного нерва лоскуты связки сопоставляли малыми основаниями и соединяли друг с другом. Ладонный апоневроз и кожу сшивали отдельными швами.
Таким образом, первоначальный этап операции, предусматривавший выполнение разрезов кожи и ладонного апоневроза, во всех клинических наблюдениях был однотипным. Последующие этапы различались в зависимости от выявленных анатомических особенностей запястного канала и патологических изменений в морфологических структурах, входящих в его состав. Заключительный этап (наложение швов на апоневроз и кожу) был также одинаковым.
В послеоперационный период всех пациентов вели в соответствии с принципами, описанными нами ранее [19].
Все пациенты до начала лечения подписывали информированное согласие на на участие в исследовании и публикацию данных в открытом доступе. Работа одобрена Комитетом по биоэтике при Самарском государственном медицинском университете (протокол № 312 от 25 ноября 2025 г.) и проведена в соответствии с Хельсинкской декларацией 1975 г. (пересмотр 2008 г.). Информацию о персональных данных пациентов не отражали.
РЕЗУЛЬТАТЫ
При внутригрупповом сравнении динамика клинико-функциональных показателей у пациентов всех трех групп в целом была положительной, что в наибольшей степени проявилось через шесть месяцев после операции. Однако в каждой группе выявлены свои особенности.
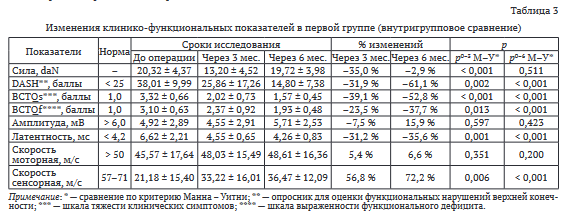
Так, в первой группе (табл. 3) величина силового захвата кисти через три месяца уменьшилась на 35,0 % (р0-3 < 0,001), а через шесть месяцев возросла, но не достигла исходного уровня. Показатель повседневной активности конечности по анкете DASH через три месяца улучшился на 31,9 % (р0-3 = 0,002), но особо значимо изменился через шесть месяцев, — на 61,1 % (р0-6 < 0,001). Аналогичную тенденцию наблюдали при оценке выраженности клинических симптомов и функциональных нарушений. Так, показатель BCTOs через шесть месяцев изменился в положительную сторону на 52,8 % (р0-6 < 0,001), а показатель BCTOf — на 37,7 % (р0-6 < 0,001). Из параметров ЭНМГ заслуживало внимания укорочение через шесть месяцев величины дистальной моторной латентности на 35,6 % (р0-6 < 0,001) и увеличение сенсорной скорости на 72,2 % (р0-6 < 0,001), что объективно подтверждало клиническую эффективность декомпрессии срединного нерва.
Динамика показателей у пациентов второй группы (табл. 4) несколько отличалась от первой группы. В частности, мы не наблюдали существенного снижения силы захвата кисти через три месяца после операции. Уменьшение составило всего лишь 9,6 % от исходного уровня (р0-3 = 0,035). Но далее, через шесть месяцев, сила захвата по сравнению с дооперационной величиной увеличилась на 15,2 % (р0-6 = 0,025). Данные клинических тестов планомерно улучшались на всех сроках наблюдения, демонстрируя значимое увеличение также через шесть месяцев: повседневная активность конечности по анкете DASH улучшилась на 70,5 % (р0-6 < 0,01), BCTOs — на 56,3 % (р0-6 < 0,01) и BCTOf — на 47 % (р0-6 < 0,001). Аналогичную тенденцию прослеживали и при анализе показателей ЭНМГ. Амплитуда М-ответа короткой мышцы, отводящей большой палец, возросла на 34,3 % (р0-6 = 0,008), дистальная моторная латентность изменилась в положительную сторону на 31,7 % (р0-6 < 0,001), а сенсорная скорость — на 72,4 % (р0-6 < 0,001).
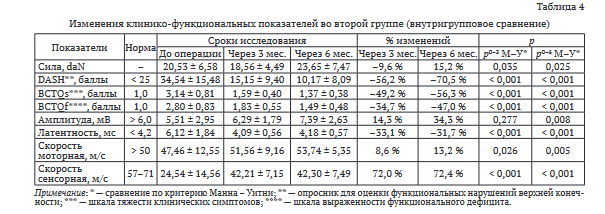
Пациенты третьей группы (табл. 5) демонстрировали еще меньшую, чем в первой и во второй группах, потерю силы захвата кисти через три месяца после операции, — всего лишь на 2 % (р0-3 = 0,935), и наибольший ее прирост через шесть месяцев, — на 24 % (р0-6 = 0,05). Значимым было увеличение функциональной активности конечности по шкале DASH, прирост которой через шесть месяцев составил 76,9 % (р0-6 < 0,001). Также у пациентов третьей группы через шесть месяцев наибольшим было улучшение по анкете BCTOs, согласно которой прирост положительной динамики был равен 61,8 % (р0-6 < 0,001), а по анкете BCTOf — 51,2 % (р0-6 < 0,001).
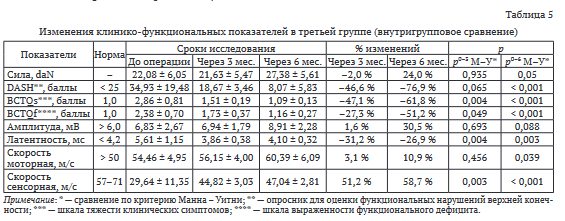
Показатели ЭНМГ имели тенденцию к нормализации, — через шесть месяцев укорочение дистальной моторной латентности составило 26,9 % (р0-6 = 0,004), а прирост моторной и сенсорной скоростей соответственно — 10,9 % (р0-6 = 0,039) и 58,7 % (р0-6 < 0,001). Следует отметить, что величины прироста этих показателей ЭНМГ у пациентов третей группы были меньше, чем у пациентов первой и второй групп, что, вероятнее всего, связано с более высокими/лучшими их дооперационными величинами.
При сравнении клинико-функциональных показателей в межгрупповом ракурсе констатировали, что сила захвата кисти через три месяца после операции снизилась у пациентов всех трех групп (рис. 2, а). Но в наибольшей степени она уменьшилась в первой группе (на 35 %), достоверно отличаясь от второй и третьей групп (р1-2, 1-3 < 0,001). При этом различий между второй и третьей группами не было. К шестому месяцу средняя величина силового захвата кисти возросла у всех. Однако, если во второй и третьей группах она существенно превысила исходные данные (на 15,2 % и 24 % соответственно), то в первой группе оставалась на 2,9 % меньше, чем до операции, достоверно различаясь со второй (р1-2 = 0,006) и третьей (р1-3 < 0,001) группами.
Повседневная активность верхней конечности, оцененная по анкете DASH, улучшалась более равномерно, чем сила захвата кисти (рис. 2б). В первой группе через шесть месяцев верхняя конечность стала более функциональной на 61,1 %, во второй — на 70,5 % и в третьей — на 76,9 %. При этом различия между первой и второй, между первой и третьей группами были статистически значимыми (р1-2 = 0,014 и р1-3 = 0,005).
Степень тяжести клинических симптомов по анкете BCTOs уменьшалась в основном также планомерно (рис. 2, в). Через шесть месяцев у пациентов первой группы она понизилась на 52,8 %, второй — на 56,3 % и третьей — на 61,8 %. При этом, если между первой и второй группами достоверных различий не наблюдали, то между первой и третьей различия были статистически значимыми (р1-3 < 0,001).
Динамика функциональных нарушений по анкете BCTOf была также положительной (рис. 2, г). Через шесть месяцев в первой группе она улучшилась на 37,7 %, во второй — на 47,0 % и в третьей — на 51,2 %. Различия между первой и второй группами, равно и как между первой и третьей группами, были статистически достоверными (р1-2, 1-3 < 0,001).
Наряду с клиническими данными показатели ЭНМГ также претерпели ряд существенных изменений, свидетельствовавших о равномерном улучшении функционального статуса кисти. Величина амплитуды М-ответа короткой мышцы, отводящей большой палец, во всех группах возрастала (рис. 2, д). Через шесть месяцев в первой группе она улучшилась на 15,9 %, во второй — на 34,3 % и в третьей на 30,5 %. Различия между первой и третьей группами были статистически значимыми (р1-3 = 0,008).
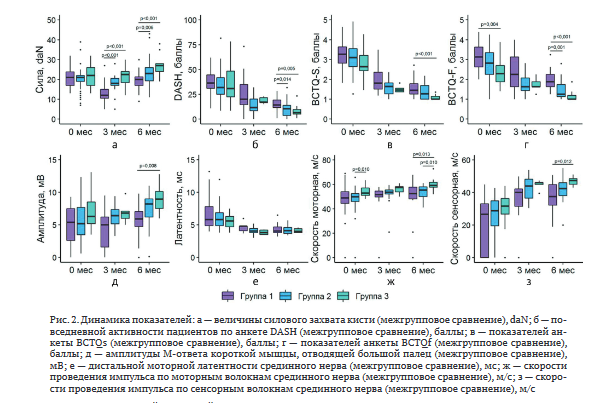
Показатель дистальной моторной латентности срединного нерва на всех этапах исследования и во всех группах также имел положительную динамику (рис. 2, е). Особо наглядно эта закономерность проявилась через три месяца, улучшив показатель у всех практически на одну треть: на 31,2 % в первой, на 33,1 % во второй и на 31,2 % в третьей группе. Однако через шесть месяцев произошло разобщение этой однонаправленной динамики. Если в первой группе дистальная моторная латентность продолжала прогрессивно сокращаться, достигнув 35,6 % от исходного, то во второй и третьей группах динамика была не так выражена
Так, по сравнению с исходным уровнем во второй группе улучшение составило 31,7 %, а в третьей — 26,9 %. Несмотря на это, моторная латентности во второй и третьей группах вернулась к нормальным величинам (< 4,2 мс).Скорость проведения импульса по моторным волокнам срединного нерва также постепенно нарастала у всех пациентов (рис. 2, ж). Через шесть месяцев после операции она увеличилась на 6,6 % в первой группе, на 13,2 % — во второй и на 10,9 % — в третьей. При этом различия между первой и второй, между первой и третьей группами были статистически значимыми с величиной достоверности р1-2 = 0,013 и р1—3 = 0,01.
Скорость проведения нервного импульса по сенсорным волокнам срединного нерва аналогично предыдущим показателям ЭНМГ также улучшалась (рис. 2, з). Своеобразный ее «скачок» произошел практически у всех пациентов через три месяца после операции: в первой группе она возросла на 56,8 %, во второй — на 72,0 % и третьей — на 51,2 %. Наряду с этим, прирост скорости через шесть месяцев был не столь очевидным. Разница в приросте скорости между группами в различные сроки была незначительна, что свидетельствует о клинической эффективности всех трех оперативных методик.
Осложнения
У двух пациентов первой группы через 1,5 месяца после операции диагностировали pillar pain, которая самостоятельно купировалась. У двух пациентов второй и двух пациентов третьей группы через один месяц возникла непродолжительная боль в послеоперационном рубце, что, возможно, было связано с неполным удалением кожных швов в амбулаторных условиях.
Таким образом, после оперативного лечения у пациентов всех трех групп наступило клинически значимое улучшение. Однако по выраженности изменения результатов динамометрии, анкетирования и ЭНМГ можно сделать заключение о более быстром и более полноценном восстановлении функции кисти у пациентов второй и третьей групп, которое начало проявляться через три месяца и приобрело наиболее выраженный и стойкий характер через шесть месяцев после операции.
Приводим клинический пример пациентки второй группы, которой выполнили открытую декомпрессию запястного канала с рефиксацией мышц тенара по разработанному нами способу.
Больная 47 лет, юрист, обратилась с жалобами на нарушение чувствительности и боль в 1—11—111 пальцах правой кисти, усиливающиеся в утренние часы, а также после занятий йогой, что постепенно нарастало в течение трех лет. Умеренно выраженная боль в кисти и чувство онемения в пальцах были преимущественно «ночными», от чего пациентка просыпалась четыре-пять раз. Кроме этого, по утрам появлялся отек кисти, движения пальцами становились затрудненными. Профессиональная, бытовая и спортивная активность существенно снизились. В последние месяцы лечилась консервативно с незначительным улучшением.
При первичном обследовании: Внешний вид правой кисти не изменен. Гипотрофии мышц тенара нет. Объем движений пальцами — полный. Болезненность в проекции запястного канала с иррадиацией в I—II—III пальцы. Тесты Тинеля и Фалена — «положительные». Сила кулачного захвата — 22 daN. Повседневная активность по шкале DASH — 32,5 балла. Результаты по опросникам BCTOs и BCTOf — 2,55 и 2,88 баллов соответственно. При ЭНМГ выявлены изменения, характерные для СЗК: амплитуда М-ответа короткой мышцы, отводящей большой палец, — 7,2 мВ; дистальная латентность моторных волокон срединного нерва — 4,6 мс; скорость проведения импульса по моторным волокнам срединного нерва — 51,3 м/с; скорость проведения импульса по сенсорным волокнам срединного нерва — 34 м/с. Результаты УЗИ: площадь поперечного сечения (ППС) срединного нерва в запястном канале увеличена (16 мм2 при норме < 11 мм2 [20]).
В сентябре 2024 г. на правой кисти выполнили операцию, в ходе которой выявили, что мышцы тена- ра занимают более половины площади передней поверхности ПСЗ. Провели открытую декомпрессию срединного нерва с рефиксацией мышц возвышения большого пальца по разработанному нами способу. Невропатическая боль перестала беспокоить на второй день. Пациентка скрупулёзно выполняла все рекомендации. Послеоперационный период прошел без осложнений. Рана зажила первичным натяжением.
При обследовании через шесть месяцев: Жалоб не предъявляет, вернулась к занятиям йогой. Трудоспособность по профессии сохранена. Ощущений онемения и покалывания в кисти нет. Боль в покое и при нагрузке отсутствует.
Объем активных движений в пальцах кисти — полный (рис. 3, а). Сила кулачного захвата — 26 daN (рис. 3, б). Функциональный статус конечности и повседневная активность по шкале DASH — 0,83 балла. По шкале BCTO — положительная динамика: BCTOs — 1,0 балла, а BCTOf — 1,0 балла. Результатами лечения удовлетворена.

При ЭНМГ выявлено улучшение показателей: амплитуда М-ответа короткой мышцы, отводящей большой палец — 8,6 мВ; дистальная латентность моторных волокон срединного нерва — 3,2 мс; скорость проведения импульса по моторным волокнам срединного нерва — 51,5 м/с; скорость проведения импульса по сенсорным волокнам срединного нерва — 49 м/с (рис. 4).
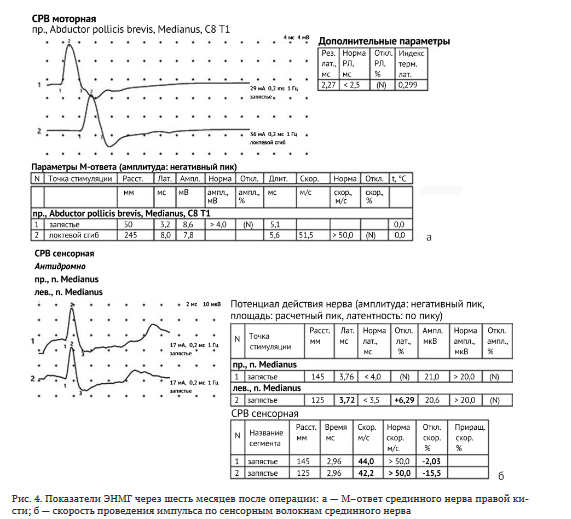
Результат УЗИ: ППС срединного нерва в запястном канале — 8 мм2 (рис. 5).
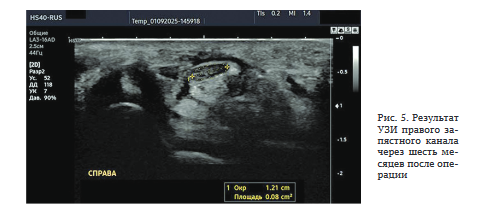
Таким образом, данное клиническое наблюдение иллюстрирует положительный результат своевременного, адекватного оперативного вмешательства по поводу идиопатического СЗК, в результате которого мышцы тенара, занимавшие более половины передней поверхности ПСЗ, фактически были сохранены, — первоначально аккуратно отслоены от связки, а затем заново прикреплены к ней.
ОБСУЖДЕНИЕ
Эффективность хирургической декомпрессии срединного нерва у пациентов с СЗК подтверждена рядом клинических исследований. Так, А.В. Гильвег с соавт. отметили выраженное уменьшение боли и других невропатических расстройств через один месяц после операции, а существенное улучшение функционального состояния кисти - через шесть месяцев [21].
В литературе также описаны нежелательные явления и осложнения после открытой декомпрессии срединного нерва. В частности, Ю.В. Беляков с соавт. выделили основные недостатки этого способа хирургического лечения пациентов с СЗК, — высокую вероятность вовлечения нервного ствола в рубец, ущемление срединного нерва краями рассеченной связки, хроническую его травматизацию у лиц, занятых ручным трудом [22]. G.M. Gartsman et al. обнаружили, что после такой операции увеличение ширины запястной дуги более чем на 20 % коррелирует со снижением силы захвата кисти на 25,8 % [23]. R. Luchetti и P. Amadio констатировали, что пересечение ПСЗ при открытой декомпрессии срединного нерва вызывает снижение силы захвата кисти в 16-25 % клинических наблюдений [24]. По утверждению А. Lluch, M. Castro-Menendez et al., W.H. Seitz et al. это обосновывает целесообразность реконструкции ПСЗ, способствующей более быстрому и полноценному восстановлению функции кисти за счет увеличения силы захвата и снижения риска возникновения боли в области послеоперационного рубца и pillar pain [4, 7, 25]. D. Netscher et al., измеряя силу захвата кисти, выявили, что у пациентов, которым восстанавливали ПСЗ, максимальная сила грубого и тонкого захватов достигала исходных величин через три месяца после операции, что достоверно превосходило аналогичные показатели у пациентов без пластики [26]. Результаты исследования Г.П. Котельникова с соавт. также подтвердили эффективность реконструкции ПСЗ, что при умеренно выраженном СЗК проявилось увеличением силы хвата кисти, улучшением показателей по опросникам BCTOs и BCTOf, данных ЭНМГ, особенно у пациентов 18-60 лет [27].
T. Mujadzic et al. отметили четырехкратное снижение частоты и длительности проявления pillar pain у пациентов при использовании мини-инвазивного хирургического доступа (7,2 %) по сравнению со стандартным разрезом (32,1 %) [5]. W.H. Seitz et al. обнаружили двукратное уменьшение частоты возникновения pillar pain и увеличение силы захвата кисти у пациентов после реконструкции ПСЗ (19 %), в сравнении с пациентами без ее пластики (8,6 %) [25]. A. Kumar et al. установили статистически значимое уменьшение частоты pillar pain через три-шесть месяцев после минимально инвазивного рассечения ПСЗ (р = 0,41). Однако в более отдаленные сроки результаты наблюдений не достигли статистически значимых величин [28].
По утверждению R.A. Bernstein et al., для профилактики pillar pain важно восстановление целостности ладонного апоневроза. Его ушивание после открытой декомпрессии сводит риск ее появления к минимуму [29]. В нашем исследовании ладонный апоневроз ушивали у пациентов всех трех групп. Это позволило сократить сроки возврата силового захвата кисти, предотвратить подвывих сухожилий сгибателей и рубцевание срединного нерва. Кроме этого, такой шаг дал возможность минимизировать частоту pillar pain. В первой группе она развилась только в двух клинических наблюдениях, а во второй и третьей ее не было вовсе.
N. Hollevoet et al. при кадаверном исследовании выявили, что место прикрепления мышц тенара к ПСЗ в ряде клинических наблюдений находилось в проекции локтевой стороны срединного нерва или было значительно смещено кнутри. В некоторых случаях ладонная поверхность ПСЗ была на 85 % покрыта мышцами тенара [9]. F. Alsafar et al. отметили, что 50 % лучевой поверхности связки занимают мышцы возвышения большого пальца (тенара), в ряде случаев лежащие на пути линии ее рассечения [8]. В настоящей работе мы установили, что место прикрепления мышц тенара к ПСЗ в 40 (43,5 %) клинических наблюдениях находилось на ее локтевой части. Все они составили вторую группу, пациентам которой выполнили открытую декомпрессию срединного нерва с рефиксацией этих мышц.
M. Jegal et al. обратили внимание на то, что в клинической практике нередко вся поверхность ПСЗ бывает покрыта мышцами тенара. В таких случаях выполнение релиза запястного канала требует рассечения брюшек этих мышц, что повышает риск повреждения моторной ветви срединного нерва, которая может иметь чрезсвязочный вариант строения. Авторы рекомендовали отслаивать мышцы тенара в лучевую сторону, чтобы можно было пересечь ПСЗ по локтевой части запястного канала, попутно проведя ревизию срединного нерва и его мышечной ветви, избежав их ятрогенного повреждения [10]. D.P. Green и J. Morgan описали случаи расположения мышц тенара на локтевой части ПСЗ, что, по мнению авторов, в 90 % случаев является косвенным признаком аномального отхождения моторной ветви срединного нерва, которую легко повредить при пересечении этих мышц [30]. T.C. Chern et al. констатировали, что при пересечении ПСЗ мышцы тенара теряли точку прикрепления, происходила их атрофия, функция кисти снижалась. Так, укорочение поверхностной головки m. flexor pollicis brevis составило 25 % (относительно длины покоя), локтевой части m. abductor pollicis brevis — 20 % (opposition and adduction), m. opponens pollicis — 20 % и m. opponens digiti minimi — 10 % [11]. По мнению F.K. Fuss и T.F. Wagner, это также является одной из причин возникновения pillar pain в послеоперационном периоде [2].
Применив на практике разработанный нами способ декомпрессии срединного нерва с рефиксацией мышц тенара и оценивая его ближайшие и отдаленные результаты, мы не наблюдали ни клинических, ни ЭНМГ-признаков повреждения моторной ветви срединного нерва. Ни у кого не возникла pillar pain. Восстановление точки прикрепления мышц тенара способствовало приросту силы захвата кисти через шесть месяцев после операции на 15,2 %, улучшению показателей опросников DASH на 70,5 %, BCTO-s — на 56,3 %, BCTO-f — на 47 %, увеличению амплитуды М-ответа короткой мышцы, отводящей большой палец на 34,3 %, уменьшению дистальной латентности моторных волокон срединного нерва на 31,7 %, увеличению моторной скорости на 13,2 % и сенсорной скорости на 72,4 % по сравнению с величинами этих показателей до операции. Эти данные свидетельствуют о положительном влиянии на конечные результаты примененного нами способа рефиксации мышц тенара в случаях, когда они занимают более половины передней поверхности ПСЗ.
Итак, дифференцированный подход к выбору способа хирургического лечения наших пациентов с СЗК обеспечил достижение высокоуровневого положительного результата у пациентов всех трех групп. Вместе с этим, факт не столь позитивно проявленных и статистически достоверно не отличающихся промежуточных и конечных результатов у пациентов первой группы по сравнению с пациентами второй и третьей групп может быть связан с более совершенной техникой оперативных вмешательств во второй и третьей группах. С другой стороны, это может быть обусловлено более часто встречающейся выраженной степени тяжести СЗК в первой группе (41,1 % против 37,5 % во второй и 38,4 % в третьей группах), но без статистически достоверных различий (табл. 2).
ЗАКЛЮЧЕНИЕ
Открытая декомпрессия срединного нерва при СЗК, выполненная нами у пациентов всех трех групп, позволила через шесть месяцев после операции достигнуть значимого клинического и функционального улучшения во всех клинических наблюдениях.
У большинства пациентов, которым после декомпрессии срединного нерва рефиксировали мышцы тенара (вторая группа) и выполнили пластику ПСЗ (третья группа) по предложенным нами способам, восстановление клинических, функциональных и ЭМНГ-показателей начало происходить через три месяца, а значимо улучшилось через шесть месяцев по сравнению с пациентами, которым пластику ПЗК не выполняли (первая группа).
При осуществлении дифференцированного подхода к выбору способа открытой декомпрессии срединного нерва при СЗК необходимо учитывать анатомические особенности запястья, выраженность патологических изменений в этой зоне, возрастные и профессиональные характеристики пациентов.
СПИСОК ИСТОЧНИКОВ
Пешин С.Е., Каракулова Ю.В., Няшин Ю.И., Няшин М.М. Синдром запястного канала с точки зрения биомеханики. Обзор литературы. Российский журнал биомеханики. 2022;26(2):13-18.
Fuss FK, Wagner TF. Biomechanical alterations in the carpal arch and hand muscles after carpal tunnel release: a further approach toward understanding the function of the flexor retinaculum and the cause of postoperative grip weakness. Clin Anat. 1996;9(2):100- 108
Ludlow KS, Merla Jl, Cox JA, Hurst LN. Pillar pain as a postoperative complication of carpal tunnel release: a review of the literature. JHand Ther. 1997;10(4):277-282. doi: 10.1016/s0894-1130(97)80042-7.
Lluch A. Reconstruction of the flexor retinaculum. In: Luchetti, R., Amadio, P. (eds) Carpal Tunnel Syndrome. Springer, Berlin, Heidelberg.; 2002:226-238. doi: 10.1007/978-3-540-49008-1_32.
Mujadzic T, Friedman HI, Mujadzic MM, et al. Modified Carpal Tunnel Release: A New Approach to Minimizing Pillar Pain. Ann Plast Surg. 2021;86(6S Suppl 5):S503-S509. doi: 10.1097/SAP.0000000000002885.
Moran-Moran J, Merida-Velasco JR, Del Valle EB, Murillo-Gonzalez J. A mini-incision carpal tunnel release technique to prevent pillar pain: A technical note. Acta Orthop Traumatol Turc. 2021;55(1):73-75. doi: 10.5152/j.aott.2021.20086.
Castro-Menendez M, Pagazaurtundba-Gomez S, Pena-Paz S, et al. Z-Elongation of the transverse carpal ligament vs. complete resection for the treatment of carpal tunnel syndrome. Rev Esp Cir Ortop Traumatol. 2016;60(6):355-365. doi: 10.1016/j.recot.2016.06.007.
Alsafar F, Li ZM. Thenar and Hypothenar Muscle Coverage on the Transverse Carpal Ligament. J Wrist Surg. 2021;11(2):150-153. doi: 10.1055/s-0041-1735887.
Hollevoet N, Barbaix E, D’Herde K, et al. Muscle fibres crossing the line of incision used in carpal tunnel decompression. J Hand Surg Eur Vol. 2010;35(2):115-119. doi: 10.1177/1753193409102465.
Jegal M, Woo SJ, Lee HI, et al. Anatomical Relationships between Muscles Overlying Distal Transverse Carpal Ligament and Thenar Motor Branch of the Median Nerve. Clin Orthop Surg. 2018;10(1):89-93. doi: 10.4055/cios.2018.10.1.89.
Chern TC, Jou IM, Chen WC, et al. An ultrasonographic and anatomical study of carpal tunnel, with special emphasis on the safe zones in percutaneous release. J Hand Surg Eur Vol. 2009;34(1):66-71. doi: 10.1177/1753193408097322.
Измалков С.Н., Семенкин О.М, Братийчук А.Н., Демченко Н.А. Способ рефиксации мышц возвышения большого пальца кисти при открытой декомпрессии срединного нерва у пациентов с синдромом запястного канала. Патент РФ на изобретение № 2828980. 21.10.2024. Бюл. № 30.
Котельников Г.П., Ларцев Ю.В., Измалков С.Н. и др. Способ хирургического лечения пациентов с синдромом запястного канала. Патент РФ на изобретение № 2734176. 13.10.2020. Бюл. № 29.
Beck JD, Wingert NC, Rutter MR, et al. Clinical outcomes of endoscopic carpal tunnel release in patients 65 and over. J Hand Surg Am. 2013;38(8):1524-1529. doi: 10.1016/j.jhsa.2013.05.016.
Hudak PL, Amadio PC, Bombardier C. Development of an upper extremity outcome measure: the DASH (disabilities of the arm, shoulder and hand) [corrected]. The Upper Extremity Collaborative Group (UeCG). Am J Ind Med. 1996;29(6):602-608. doi: 10.1002/ (SICI)1097-0274(199606)29:6<602::AID-AJIM4>3.0.CO;2-L.
Розов А.В., Лила А.М., Бялик Е.И. и др. Результаты сухожильных трансферов для стабилизации суставов запястья у пациентов с ревматоидным артритом. Наука и инновации в медицине. 2024;9(4):311-316. doi: 10.35693/SIM633628.
Levine DW, Simmons Bp, Koris MJ, et al. A self-administered questionnaire for the assessment of severity of symptoms and functional status in carpal tunnel syndrome. J Bone Joint Surg Am. 1993;75(11):1585-1592. doi: 10.2106/00004623-199311000-00002.
Юсупова Д.Г., Супонева Н.А., Зимин А.А. и др. Валидация Бостонского опросника по оценке карпального туннельного синдрома (Boston Carpal Tunnel Questionnaire) в России. Нервно-мышечные болезни. 2018;8(1):38-45. doi: 10.17650/2222-8721-2018-8-1-38-45.
Семенкин О.М., Измалков С.Н., Братийчук А.Н. и др. Результаты оперативного лечения пациентов с синдромом запястного канала в зависимости от степени выраженности заболевания. Гений ортопедии. 2021;27(1):24-31. doi: 10.18019/1028-4427- 2021-27-1-24-31.
Николаев С. Г. Электромиография: клинический практикум. Иваново: ПресСто; 2019:392.
Гильвег А.С., Парфенов В.А., Евзиков Г.Ю. Ближайшие и отдаленные результаты декомпрессии срединного нерва при синдроме запястного канала. Неврология, нейропсихиатрия, психосоматика. 2018;10(3):79-85. doi: 10.14412/2074-2711-2018-3-79-85.
Беляков Ю.В., Иваненко А.В., Олейник Е.А. Осложнения хирургического лечения и причины рецидивов синдрома запястного канала. Российский нейрохирургический журнал им. профессора А.Л. Поленова. 2021;13(4):15-21
Gartsman GM, Kovach JC, Crouch CC, et al. Carpal arch alteration after carpal tunnel release. J Hand Surg Am. 1986;11(3):372-374. doi: 10.1016/s0363-5023(86)80144-7.
Luchetti R, Amadio P. Carpal Tunnel Syndrome. Berlin: Springer; 2002:121-129. doi: 10.1007/978-3-540-49008-1.
Seitz WH, Lall A Open carpal tunnel release with median neurolysis and Z-plasty reconstruction of the transverse carpal ligament. Current Orthopaedic Practice. 2013;24(1):53-57. doi: 10.1097/BCO.0b013e3182797ac3.
Netscher D, Steadman AK, Thornby J, Cohen V. Temporal changes in grip and pinch strength after open carpal tunnel release and the effect of ligament reconstruction. J Hand Surg Am. 1998;23(1):48-54. doi: 10.1016/S0363-5023(98)80088-9.
Котельников Г.П., Повелихин А.К., Князев Н.А. и др. Отдалённые результаты хирургического лечения с применением реконструкции поперечной запястной связки у пациентов с синдромом запястного канала в зависимости от возрастных категорий и степени тяжести заболевания. Вестник медицинского института «РЕАВИЗ». 2023;13(2):56-61. doi: 10.20340/vmi- rvz.2023.2.CLIN.6.
Kumar AA, Lawson-Smith M. Pillar Pain After Minimally Invasive and Standard Open Carpal Tunnel Release: A Systematic Review and Meta-analysis. J Hand Surg Glob Online. 2024;6(2):212-221. doi: 10.1016/j.jhsg.2023.12.003.
Bernstein RA. Endoscopic carpal tunnel release. Conn Med. 1994;58(7):387-94.
Green DP, Morgan JP. Correlation between muscle morphology of the transverse carpal ligament and branching pattern of the motor branch of median nerve. J Hand SurgAm. 2008;33(9):1505-1511. doi: 10.1016/j.jhsa.2008.05.025.
Информация об авторах:
Сергей Николаевич Измалков — доктор медицинских наук, профессор, заведующий кафедрой
Олег Михайлович Семенкин — кандидат медицинских наук, врач — травматолог-ортопед, доцент кафедры
Александр Николаевич Братийчук — доктор медицинских наук, профессор кафедры
Алексей Константинович Усов — кандидат медицинских наук, заведующий отделением, доцент кафедры
Никита Алексеевич Демченко — аспирант, врач — травматолог-ортопед
Алена Евгеньевна Гусева — врач функциональной диагностики
Кира Фларитовна Хайруллина — врач ультразвуковой диагностики
Теги: запястье
234567 Начало активности (дата): 27.04.2026
234567 Кем создан (ID): 989
234567 Ключевые слова: синдром запястного канала, поперечная связка запястья, оперативное лечение
12354567899
Похожие статьи
ЗапястьеРентген на дому 8 495 22 555 6 8
Рука человека
Системная реабилитация пациентов с плегией, синдромом «спастическая рука» в бытовых условиях («госпиталь на руке»)



