 02.05.2026
02.05.2026
Особенности ремоделирования суставных структур при протезировании смежного сегмента конечности имплантатомс кальций-фосфатным покрытием
Изучение особенностей реорганизации компонентов смежного с протезом сустава и определение предикторов артроза являются залогом успешного восстановления функции протезируемой конечности
ВВЕДЕНИЕ
Остеоинтегративное экзопротезирование конечностей представляет собой передовую технологию восстановления утраченных конечностей путем интеграции металлического имплантата с костной тканью культи, обеспечивая стабильное и функциональное соединение [1, 2, 3, 4]. Преимущества данного метода включают улучшение функциональности и качества жизни пациентов, сенсорной обратной связи (остеоперцепция и остеопроприорецепция), долгосрочное функционирование и устранение проблем, связанных с традиционными гильзовыми протезами (раздражение кожи, плохое прилегание, высокая частота боли в костях и/или мягких тканях, аллергические реакции, снижение функции и дальнейшее ухудшение качества жизни) [5, 6, 7, 8, 9].
Современные исследования по улучшению остеоинтегративных свойств имплантатов направлены на повышение эффективности срастания костной ткани с имплантатом путем модификации его поверхности (микротекстурирование, наноструктурные и биологически активные покрытия), стимуляции остеогенеза (электростимуляция, применение препаратов, стимулирующих минерализацию) [10, 11, 12, 13].
Установлено, что имплантаты с кальций-фосфатным покрытием обладают высокой биосовместимостью, ускоряют процесс остеоинтеграции [14, 15].
Исследования на животных показали, что в смежном суставе через шесть месяцев после протезирования голени имплантатом типа PressFit структурные изменения суставного хряща соответствовали степени 0-1 по классификации Международного общества изучения остеоартроза OARSI [16]. Структурные изменения субхондральной зоны по классификации O-M. Aho et al. [17] соответствовали стадии 0, — «очень ранние признаки остеоартроза» [18]. При установке имплантатов с кальцийфосфатным покрытием в выше расположенном суставе процессы резорбции субхондральной кости и истончение суставного хряща были выражены в меньшей степени по сравнению с имплантатами без покрытия [19].
У пациентов, перенесших ампутацию конечности, распространенным осложнением после протезирования являются контрактуры и артроз в смежном суставе, возникающие из-за таких факторов как повышенная нагрузка на сустав, нарушение биомеханики, длительная неподвижность суставов, мышечная слабость и воспалительная реакция организма на имплантаты [20, 21].
Нарушение нормальной биомеханики сустава, наличие очагов инфекции, которые встречаются после протезирования конечности [5], относятся к основными причинами развития синовита [22].
Цель работы — оценить структурную реорганизацию основных компонентов сустава в отдаленные сроки после протезирования голени имплантатом с кальций-фосфатным покрытие
Изучение особенностей структурной реорганизации компонентов смежного с протезом сустава и определение предикторов артроза являются залогом успешного восстановления функции протезируемой конечности и долгой службы протеза.
МАТЕРИАЛ И МЕТОДЫ
Дизайн исследования
Исследование выполнено на 11 беспородных собаках (самцы) в возрасте (1,8 ± 0,5) лет, с массой тела (19,0 ± 1,2) кг. Опытным животным (n = 6) моделировали культю большеберцовой кости на уровне верхней трети диафиза. Через 2,5 месяца устанавливали имплантат из сплава Ti6Al4V с кальцийфосфатным покрытием (Патент на полезную модель РФ № 194912, [23]). Затем с помощью аппарата Илизарова и специального устройства (Патент РФ №185647, [24]) имплантат фиксировали и создавали компрессию на кость (Бн = 20 Н) в течение 35 дней после операции, затем устанавливали экзопротез. Этапы исследования — шесть и 12 месяцев после протезирования.
Объекты исследования: синовиальная оболочка, суставной хрящ и субхондральная зона большеберцового плато.
В качестве контроля исследовали синовиальную оболочку, суставной хрящ и субхондральную зону большеберцового плато пяти интактных собак.
Этические принципы
Исследование проведено в соответствии с правилами Европейской конвенцией (ETS № 123) о защите позвоночных животных, используемых для экспериментов или в иных научных целях и межгосударственным стандартам (ГОСТ 33044-2014). Исследование одобрено локальным этическим комитетом (протокол от 29.11.2024 № 1(76)).
Эвтаназия
Эвтаназию осуществляли после миорелаксации раствором димедрола 1 % (0,02 мг/кг) и рометара 2 % (5 мг/кг) введением летальной дозы барбитуратов.
Гистологические методы исследования
Для гистоморфометрического исследования вскрывали коленный сустав, иссекали фрагменты синовиальной оболочки, с нагружаемых участков большеберцового плато вырезали образцы суставного хряща с подлежащей субхондральной костью. Вырезанные костно-хрящевые блоки фиксировали в 10 % растворе нейтрального формалина, затем декальцинировали в смеси растворов муравьиной и соляной кислот (применяли стандартный протокол щадящей декальцинации, при котором декальцинация значимо не влияла на тинкториальные свойства костного матрикса). Дальнейшие этапы парафиновой проводки костно-хрящевых блоков осуществляли в аппарате для вакуумной проводки тканей HlSTOSAFETM INFILTRATM (ООО «ЭргоПродакшн», Россия). Срезы толщиной 5-7 мкм с парафиновых блоков изготавливали на микротоме НМ 450 Thermo Scientific (США), затем окрашивали гематоксилином и эозином, для выявления степени минерализации костного матрикса применяли специальную окраску трехцветным методом по Массону [25].
Для анализа ангиогенеза проводили иммуногистохимическое исследование на определение наличия маркера CD34 (моноклональные антитела кролика к CD34 [EP373Y]) (Abcam, Великобритания). Для визуализации реакции применяли набор реагентов для иммуногистохимической детекции HRP/DAB (ab236469 — Rabbit specific HRP/DAB Detection IHC Detection Kit-Micropolymer, Abcam, Великобритания). Все этапы постановки реакции проводили согласно протоколу фирмы-производителя антител. Срезы докрашивали гематоксилином.
Образцы синовиальной оболочки после альдегидно-осмиевой фиксации обезвоживали и заключали в двухкомпонентную эпоксидную смолу. Полутонкие (0,5-1,0 мкм) срезы (4-8 мм2) готовили на ультрамикротоме Nova (LKB, Швеция), окрашивали метиленовым синим и основным фуксином.
Исследование на светооптическом уровне производили с помощью микроскопа AxioScope.A1 с цифровой камерой AxioCam (CarlZeissMicrolmagingGmbH, Германия).
При гистоморфометрии с использованием ПО Zenblue (CarlZeissMicrolmagingGmbH, Германия) в суставном хряще определяли параметры: толщина некальцифицированного хряща (huncai.cr, мкм), толщина кальцифицированного хряща (hcal.cr, мкм). В глубокой зоне некальцифицированного хряща оценивали частоту встречаемости сосудов (отношение суммы сосудов в полях зрения к количеству всех анализируемых полей зрения), от каждого животного анализировали в среднем 20 полей при увеличении 400*. В субходральной зоне определяли толщину субхондральной костной пластики (haTh, мкм), рассчитывали костный индекс как отношение толщины трабекул (TbTh, мкм) к ширине межтрабекулярных пространств (ItTh, мкм).
Выраженность структурных изменений суставного хряща оценивали согласно гистологической классификации OARSI [16], структурные изменения субхондральной зоны — по классификации O-M. Aho et al. [17], выраженность воспалительного процесса в синовиальной оболочке — по шкале V. Krenn et al. [26].
Статистические методы
Количественные данные обрабатывали в табличном процессоре Microsoft Exсel. Оценку типа распределения выборок проводили с помощью критерия Колмогорова. Мера центральной тенденции параметров представлена в виде медианы и квартилей, минимальных и максимальных значений (Me (р25-р75) [min-max]) и в виде средней и ошибки средней (М ± m). Для анализа различий сравниваемых групп использовали критерий Манна - Уитни, для частотных показателей — критерий Барнарда, значимыми считали различия при р < 0,05 (программа AtteStat, версия 9.3.1).
РЕЗУЛЬТАТЫ
Структурная реорганизация синовиальной оболочки
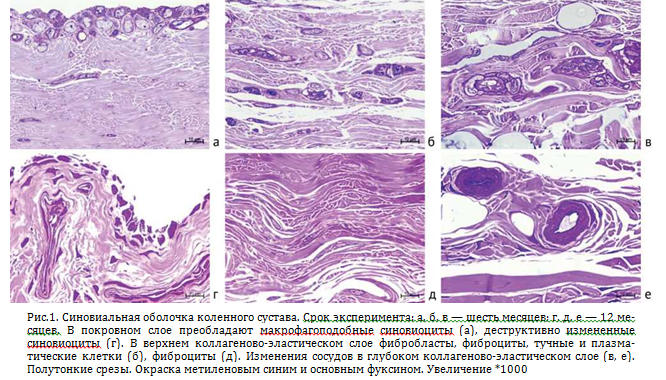
Через шесть месяцев эксперимента в синовиальной оболочке в покровном слое синовиальные клетки располагались в один-три слоя, преобладали макрофагоподобные синовиоциты, такие клетки имели овоидное ядро, цитоплазматические выросты, базофильную цитоплазму, содержащую множество гранул и вакуолей (рис. 1, а). В поверхностном коллагеново-эластическом слое преобладали коллагеновые волокна, клеточность была умеренно повышена, наряду с фиброцитами и фибробластами регистрировали плазматические клетки, скопления тучных клеток (рис. 1, б). В глубоком коллагеново-эластическом слое регистрировали сосуды с утолщенными стенками за счет гипертрофии гладкомышечных клеток, в отдельных сосудах набухшие ядра эндотелиальных клеток перекрывали внутрисосудистое пространство (рис. 1, в).
Через 12 месяцев эксперимента отмечали участки утолщения покровного слоя, в которых синовиальные клетки располагались в три-четыре слоя, основная часть синовиоцитов — с признаками деструкции, аномальной формы с пикнотичными ядрами (рис. 1, г). В поверхностном коллагеновоэластическом слое сохранялись нормальная клеточность и единично расположенные фибробласты, фиброциты (рис. 1, д), отмечено увеличение оптических пустот между волокнами. В глубоком коллагеново-эластическом слое сосуды — с утолщенными стенками и стенозом (рис. 1, е).
Структурная реорганизация суставного хряща
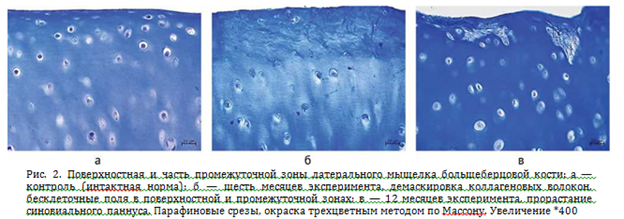
Суставной хрящ мыщелков большеберцовой кости в эксперименте, как и в контроле, сохранял зональное строение, четко определялись все зоны хряща. В поверхностной зоне через шесть месяцев эксперимента в большей части наблюдений отмечено уменьшение доли клеточного компонента и увеличение доли бесклеточных полей, нарушение гомогенности межклеточного вещества (рис. 2, б). Через 12 месяцев эксперимента в одном наблюдении из трех отмечена инвазия синовиального паннуса в поверхностную зону хряща, пустые клеточные лакуны (рис. 2, в).
На протяжении всего эксперимента в промежуточной и глубокой зонах сохранена цитоархитектоника, отмечены бесклеточные поля, часть клеток — с признаками хондроптоза.
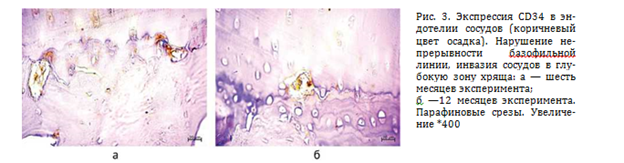
Регистрировали участки нарушения непрерывности базофильной линии и инвазию сосудов и костно-мозгового паннуса в глубокую зону некальцифицированного хряща (рис. 3). Частота встречаемости сосудов в глубокой зоне через шесть месяцев эксперимента составила (0,35 ± 0,02), через 12 месяцев — (0,30 ± 0,02), различия статистически незначимы (р = 0,736).
Структурная реорганизация субхондральной зоны
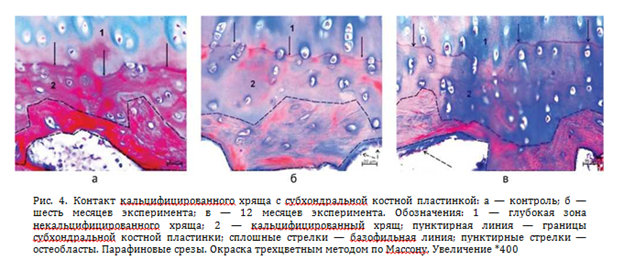
У интактных животных (контроль) субхондральная костная пластинка — неравномерной толщины, непрерывна, в костном матриксе при окрашивании трехцветным методом по Массону преобладали фуксинофильные структуры (рис. 4, а). В экспериментальной серии толщина субхондральной костной пластинки варьировала, в шесть месяцев эксперимента чаще выявляли участки истончения, в 12 месяцев эксперимента — участки утолщения. При окраске трехцветным методом по Массону через шесть месяцев отмечали снижение доли фуксинофильных структур (рис. 4, б), а через 12 месяцев доля фуксинофильных структур вновь возрастала (рис. 4, в), что косвенно свидетельствовало о повышении минерализации костного матрикса.
На протяжении всего эксперимента регистрировали участки субхондральной костной пластинки, выстланные активными остеобластами, продуцирующими основное вещество (рис. 4, б, в).
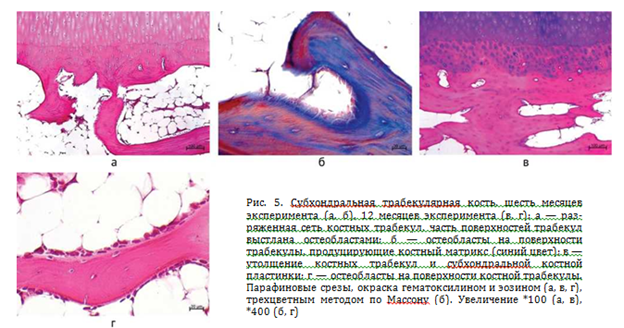
В субхондральной трабекулярной кости на всех этапах эксперимента отмечены признаки репаративного остеогенеза, — активные остеобласты, выстилающие поверхности костных трабекул (рис. 5). Сеть костных трабекул — разряженная, поверхности трабекул частично выстланы остеобластами (рис. 5, а). При окрашивании трехцветным методом по Массону матрикс костных трабекул имеет преимущественно красный цвет (рис. 5, б). Костных трабекулы и субхондральная костная пластинка утолщены (рис. 5, в). На поверхности костной трабекулы присутствуют остеобласты (рис. 5, г).
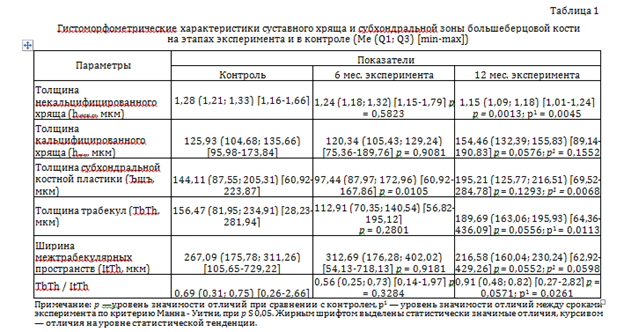
Гистоморфометрический анализ через шесть месяцев эксперимента не выявил относительно контроля статистически значимых различий значений параметров толщины некальцифицированного и кальцифицированного хряща, отмечено статистически значимое снижение толщины субхондральной костной пластинки, различия значений костного индекса в субхондральной трабекулярной кости — на уровне статистической тенденции (табл. 1).
Через 12 месяцев эксперимента при сравнении с контролем регистрировали статистически значимое снижение значений толщины некальцифицированного хряща, увеличение значений толщины кальцифицированного хряща на уровне статистической тенденции. В субхондральной зоне медиана толщины субхондральной костной пластинки больше контроля на 33 %, медиана костного индекса в субхондральной трабекулярной кости на 31 %, различия с контролем — на уровне статистической тенденции, различия между сроками эксперимента статистически значимы (табл. 1).
При использовании морфологических шкал оценка синовиальной оболочки по шкале V. Krenn et al. [26] указывала на слабо выраженный синовит у всех животных через шесть месяцев эксперимента и в 30 % наблюдений через 12 месяцев эксперимента (в 70 % наблюдений синовит не выявлен). Структурные изменения суставного хряща по шкале OARSI [16] через шесть месяцев эксперимента в большей части наблюдений соответствовали 1 степени (в 30 % — нулевой степени), через 12 месяцев в 70 % наблюдений — 1 степени, в 30 % — 2 степени.
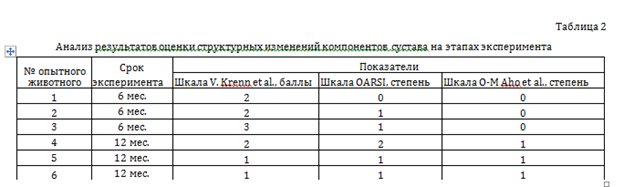
Структурные изменения субхондральной зоны по шкале O-M. Aho et al. [17] через шесть месяцев эксперимента соответствовали нулевой степени, — «очень ранние изменения», когда субхондральный склероз отсутствует, а субхондральная костная пластинка истончена. Через 12 месяцев эксперимента увеличение медианы толщины субхондральной костной пластинки и увеличение объёма трабекулярной кости свидетельствовали об очаговом субхондральном склерозе и соответствовали 1 степени (табл. 2).
ОБСУЖДЕНИЕ
В выполненном исследовании впервые проведена комплексная оценка структурной реорганизации основных компонентов сустава при экзопротезировании смежного сегмента конечности имплантатом с кальций-фосфатным покрытием в отдаленные сроки после протезирования.
Согласно современным представлениям, первоначальные изменения при остеоартрите, возникающие при макро- или микроповреждениях, происходят на молекулярном уровне, активируют патологические адаптивные восстановительные ответы, включая провоспалительные пути иммунной системы [27]. Известно, что синовиальная среда при остеоартрите характеризуется гиперплазией синовиальной оболочки, формированием синовиального паннуса, увеличением представительства макрофагоподобных синовиоцитов, повышенной инфильтрацией иммунных клеток. М1-поляризованные макрофаги и активированные фибробластоподобные синовиоциты и фибробласты продуцируют провоспалительные цитокины, которые, в свою очередь, отвечают за повышенный синтез и экспрессию матриксных металлопротеиназ, разрушающих суставной хрящ [28, 29]. Одновременно с изменениями в хряще регистрируют структурные изменения в подлежащей субхондральной зоне, склероз субхондральной кости, обширное ремоделирование трабекул, образование очагов некроза и остеофитов в краевых участках сустава [30].
Как показало данное исследование, через шесть месяцев после протезирования в смежном суставе в большей части наблюдений выявлен слабо выраженный синовит, который выражался гиперплазией покровного слоя, увеличением представительства макрофагоподобных синовиальных клеток, наличием в субсиновиальном слое плазматических и тучных клеток. На протяжении всего эксперимента регистрировали гистологические признаки нарушения кровоснабжения синовиальной оболочки (сужение просветов сосудов микроциркуляторного русла). Слабо выраженный синовит, выявленный в шесть месяцев эксперимента, через 12 месяцев в большей части наблюдений имел обратимый характер (сохранялся в одном наблюдении и сопровождался инвазией синовиального паннуса в поверхностную зону суставного хряща).
Гистологические признаки воспаления синовиальной оболочки в данных условиях эксперимента характерны для неинфекционного синовита [26] и могут быть обусловлены повреждением нервных волокон и/или нарушением биомеханики сустава.
При изучении биомеханических факторов остеоартрита коленного сустава E.R. Esposito et al. показали, что у пациентов с транстибиальной ампутацией повышен риск развития данного заболевания [31].
Воспаление и нарушение кровоснабжения синовиальной оболочки оказывают негативное влияние на структуру суставного хряща посредством нескольких механизмов, включая высвобождение воспалительных медиаторов, нарушение транспорта питательных веществ и вывода продуктов обмена веществ посредством диффузии [32].
На протяжении всего эксперимента отмечено врастание сосудов со стороны субхондральной зоны в глубокую зону некальцифицированного хряща. Проникновение кровеносных сосудов в хрящ является патологическим процессом, который может привести к его разрушению и замещению фиброзной и/или костной тканью. Антиангиогенные факторы, вырабатываемые хондроцитами, помогают предотвратить этот процесс. Установлено, что тяжесть повреждения суставного хряща коррелирует с количеством вновь образованных кровеносных сосудов [33, 34].
Гистоморфометрически к концу эксперимента зарегистрировано статистически значимое относительно контроля снижение значений толщины некальцифицированного хряща, при этом статистически значимо больше были значения толщины кальцифицированного хряща. В субхондральной зоне значения морфометрируемых параметров широко варьировали как в контроле, так и на протяжении всего эксперимента. К концу эксперимента медианы параметров «толщина субхондральной костной пластинки», «костный индекс в субхондральной трабекулярной кости» были больше контроля. Обнаруженная разница значений параметров толщины субхондральной костной пластинки и костного индекса субхондральной зоны по сравнению с контролем не является статистически значимой, но имеет тенденцию к проявлению (р < 0,1), что требует проведения дальнейших исследований большего размера выборки для подтверждения или опровержения этой тенденции.
При окраске трехцветным методом по Массону в субхондральной костной пластинке и субхондральной трабекулярной кости преобладали фуксинофильные структуры, поверхности костных трабекул выстилали активные остеобласты, что косвенно свидетельствовало о положительном влиянии кальций-фосфатного покрытия имплантата на процессы репаративного остеогенеза и минерализацию костного матрикса.
Субхондральный склероз при остеоартрите является результатом компенсаторно-адаптационных реакций в ответ на снижение минерализации костного матрикса, направленных на поддержание структуры гиалинового хряща при механической нагрузке и предотвращение его дальнейшей деструкции [35, 36]. Ключевым фактором остеоартрита является не сам субхондральный склероз, а усиленное ремоделирование костной ткани, снижение минерализации костного матрикса [35, 37]. Выявленные в данном исследовании гистологические признаки воспаления и нарушения кровоснабжения синовиальной оболочки, инвазия синовиального паннуса в поверхностную зону хряща, истончение суставного хряща, проникновение сосудов в глубокую зону некальцифицированного хряща со стороны субхондральной зоны являются прогностическими гистологическими маркерами остеоартрита.
Полученные знания о структурной реорганизации основных компонентов смежного с протезом сустава в отдаленные сроки после протезирования имеют большое значение для разработки оптимальной терапевтической стратегии, направленной на замедление прогрессирования остеоартрита.
ЗАКЛЮЧЕНИЕ
Структурные изменения костно-хрящевого компонента большеберцового плато через год после протезирования голени имплантатом с кальций-фосфатным покрытием соответствовали начальной стадии остеоартрита.
Неинфекционный синовит слабой степени выраженности в большей части наблюдений имел обратимый характер. Применение имплантатов с кальций-фосфатным покрытием способствовало активации процессов репаративного остеогенеза и минерализации костного матрикса в субхондральной зоне.
СПИСОК ИСТОЧНИКОВ
Li Y, Fellander-Tsai L. The bone anchored prostheses for amputees - Historical development, current status, and future aspects. Biomaterials. 2021;273:120836. doi: 10.1016/j.biomaterials.2021.120836.
Hoellwarth JS, Tetsworth K, Rozbruch SR, et al. Osseointegration for Amputees: Current Implants, Techniques, and Future Directions. JBJSRev. 2020;8(3):e0043. doi: 10.2106/JBJS.RVW.19.00043.
Wnuk-Scardaccione A, Bilski J. Breaking Barriers-The Promise and Challenges of Limb Osseointegration Surgery. Medicina (Kaunas). 2025;61(3):542. doi: 10.3390/medicina61030542.
Stock L, Seyboldt LF, Wilkens P, Braatz F. Osseointegration in amputation surgery : Representative studies. Unfallchirurgie (Heidelb). 2025;128(4):248-255. (In German) doi: 10.1007/s00113-025-01542-5.
Синегуб А.В., Коваленко Д.А., Чупряев В.А. и др. Осложнения при использовании остеоинтегративных экзопротезов и сравнение качества жизни пациентов при различных системах протезирования: обзор литературы. Травматология и ортопедия России. 2025;31(2):178-189. doi: 10.17816/2311-2905-17663.
Orgel M, Schwarze F, Graulich T, et al. Comparison of functional outcome and patient satisfaction between patients with socket prosthesis and patients treated with transcutaneous osseointegrated prosthetic systems (TOPS) after transfemoral amputation. Eur J Trauma Emerg Surg. 2022;48(6):4867-4876. doi: 10.1007/s00068-022-02018-6.
Tropf JG, Potter BK. Osseointegraton for amputees: Current state of direct skeletal attachment of prostheses. Orthoplast Surg. 2023;12:20-28. doi: 10.1016/j.orthop.2023.05.004.
Tereshenko V, Giorgino R, Eberlin KR, et al. Emerging Value of Osseointegration for Intuitive Prosthetic Control after Transhumeral Amputations: A Systematic Review. Plast Reconstr Surg Glob Open. 2024;12(5):e5850.
Mortazavi SMJ, Abbaspour A, Seyedtabaei SMM, et al. Improving quality of life for transfemoral amputees: results from a two-year study of the OPRA implant system and rehabilitation protocol. Eur J Orthop Surg Traumatol. 2025;35(1):85.
Hou C, An J, Zhao D, et al. Surface Modification Techniques to Produce Micro/Nano-scale Topographies on Ti-Based Implant Surfaces for Improved Osseointegration. FrontBioengBiotechnol. 2022;10:835008. doi: 10.3389/fbioe.2022.835008.
Pettersen E, Anderson J, Ortiz-Catalan M. Electrical stimulation to promote osseointegration of bone anchoring implants: a topical review. JNeuroengRehabil. 2022;19(1):31. doi: 10.1186/s12984-022-01005-7.
Losiewicz B, Osak P, Nowinska D, Maszybrocka J. Developments in dental implant surface modification. Coatings. 2025;15(1):109. doi: 10.3390/coatings15010109.
Ziegelmeyer T, Martins de Sousa K, Liao TY, et al. Multifunctional micro/nano-textured titanium with bactericidal, osteogenic, angiogenic and anti-inflammatory properties: Insights from in vitro and in vivo studies. Mater Today Bio. 2025;32:101710. doi: 10.1016/j.mtbio.2025.101710.
Korytkin AA, Orlinskaya NY, Novikova YS, et al. Biocompatibility and Osseointegration of Calcium Phosphate-Coated and Non- Coated Titanium Implants with Various Porosities. Sovrem TekhnologiiMed. 2021;13(2):52-57. doi: 10.17691/stm2021.13.2.06.
Стогов М.В., Еманов А.А., Кузнецов В.П., и др. Влияние цинксодержащего кальций-фосфатного покрытия на остеоинтеграцию чрескожных имплантатов для протезирования конечностей. Гений ортопедии. 2024;30(5):677-686. doi: 10.18019/1028- 4427-2024-30-5-677-686.
Pritzker KP, Gay S, Jimenez SA, et al. Osteoarthritis cartilage histopathology: grading and staging. Osteoarthritis Cartilage. 2006;14(1):13-29. doi: 10.1016/j.joca.2005.07.014.
Aho O-M, Finnila M, Thevenot J, et al. Subchondral bone histology and grading in osteoarthritis. PLoS One. 2017;12(3):e0173726. doi: 10.1371/journal.pone.0173726.
Ступина Т.А., Еманов А.А., Кузнецов В.П., Овчинников Е.Н. Оценка риска развития остеоартроза коленного сустава при протезировании голени (пилотное экспериментально-морфологическое исследование). Гений ортопедии. 2021;27(6):795-799. doi: 10.18019/1028-4427-2021-27-6-795-799.
Ступина Т.А., Еманов А.А., Кузнецов В.П., Овчинников Е.Н. Ремоделирование суставного хряща и субхондральной зоны большеберцовой кости при экзопротезировании конечности. Гений ортопедии. 2025;31(3):341-349. doi: 10.18019/1028-4427-2025- 31-3-341-349.
Bowker HK, Michael JW. Atlas of Limb Prosthetics: Surgical, Prosthetic, and Rehabilitation Principles. St. Louis: Mosby Year Book; 1992:930
Сусляев В.Г., Щербина К.К., Смирнова Л.М. и др. Ранняя протезно-ортопедическая помощь как основа медицинской реабилитации детей с врождёнными и ампутационными дефектами нижних конечностей. Гений ортопедии. 2020;26(2):198-205. doi: 10.18019/1028-4427-2020-26-2-198-205.
Mathiessen A, Conaghan PG. Synovitis in osteoarthritis: current understanding with therapeutic implications. Arthritis Res Ther. 2017;19(1):18. doi: 10.1186/s13075-017-1229-9.
Кузнецов В.П., Горгоц В.Г., Аникеев А.В. и др. Имплантат культи трубчатой кости. Патент РФ на полезную модель № 194912. 30.12.2019, Бюл. № 1. \
Кузнецов В.П., Губин А.В., Горгоц В.Г. и др. Устройство для остеоинтеграции имплантата в кость культи нижней конечности. Патент РФ на полезную модель № 185647. 13.12.2018. Бюл. № 35. \
Zhang C, Yan B, Cui Z, et al. Bone regeneration in minipigs by intrafibrillarly-mineralized collagen loaded with autologous periodontal ligament stem cells. SciRep. 2017;7(1):10519. doi: 10.1038/s41598-017-11155-7
Krenn V, Morawietz L, Burmester GR, et al. Synovitis score: discrimination between chronic low-grade and high-grade synovitis. Histopathology. 2006;49(4):358-364. doi: 10.1111/j.1365-2559.2006.02508.x.
Алексеева Л.И., Таскина Е.А., Кашеварова Н.Г. Остеоартрит: эпидемиология, классификация, факторы риска и прогрессирования, клиника, диагностика, лечение. Современная ревматология. 2019;13(2):9-21. doi: 10.14412/1996-7012-2019-2-9-21.
Раймуев К.В., Ищенко А.М., Малышев М.Е. Провоспалительные и противовоспалительные цитокины в патогенезе остеоартрита. Вестник Северо-Западного государственного медицинского университета им. И.И. Мечникова. 2018;10(3):19-27. doi: 10.17816/mechnikov201810319-27.
Дыдыкина И.С., Арутюнова Е.В., Коваленко П.С. и др. Синовит при остеоартрите: современное состояние проблемы. Современная ревматология. 2021;15(2):120-125. doi: 10.14412/1996-7012-2021-2-120-125.
Donell S. Subchondral bone remodelling in osteoarthritis. EFORT Open Rev. 2019;4(6):221-229. doi: 10.1302/2058-5241.4.180102.
Russell Esposito E, Wilken JM. Biomechanical risk factors for knee osteoarthritis when using passive and powered ankle-foot prostheses. Clin Biomech (Bristol). 2014;29(10):1186-1192. doi: 10.1016/j.clinbiomech.2014.09.005.
van der Kraan PM. The Interaction between Joint Inflammation and Cartilage Repair. Tissue Eng Regen Med. 2019;16(4):327-334. doi: 10.1007/s13770-019-00204-z.
Franses RE, McWilliams DF, Mapp PI, Walsh DA. Osteochondral angiogenesis and increased protease inhibitor expression in OA. Osteoarthritis Cartilage. 2010;18(4):563-571. doi: 10.1016/j.joca.2009.11.015.
Zhao Z, Sun X, Tu P, et al. Mechanisms of vascular invasion after cartilage injury and potential engineering cartilage treatment strategies. FASEB J. 2024;38(6):e23559. doi: 10.1096/fj.202302391RR.
Cox LG, van Donkelaar CC, van Rietbergen B, et al. Decreased bone tissue mineralization can partly explain subchondral sclerosis observed in osteoarthritis. Bone. 2012;50(5):1152-1161. doi: 10.1016/j.bone.2012.01.024.
Stewart HL, Kawcak CE. The Importance of Subchondral Bone in the Pathophysiology of Osteoarthritis. Front Vet Sci. 2018;5:178. doi: 10.3389/fvets.2018.00178.
Goetzen M, Hofmann-Fliri L, Arens D. et al. Subchondral screw abutment: does it harm the joint cartilage? An in vivo study on sheep tibiae. Int Orthop. 2017;41(8):1607-1615. doi: 10.1007/s00264-017-3404-7.
Информация об авторах:
Татьяна Анатольевна Ступина — доктор биологических наук, ведущий научный сотрудник
Андрей Александрович Еманов — кандидат ветеринарных наук, ведущий научный сотрудник
Виктор Павлович Кузнецов — доктор технических наук, профессор, заведующий лабораторией
Теги: экзопротезирование
234567 Начало активности (дата): 02.05.2026
234567 Кем создан (ID): 989
234567 Ключевые слова: экзопротезирование, имплантат с кальций-фосфатным покрытием, синовиальная оболочка, остео-хондральный компонент, морфометрия
12354567899



