 07.05.2026
07.05.2026
Сравнительный анализ результатов операции Геллера — Готтштейна до и после внедрения способа по выпрямлению вертикальной оси пищевода у пациентов с ахалазией кардии IV стадии
Ахалазия кардии IV стадии сопровождается выраженным расширением и S образной деформацией пищевода, что приводит к тяжелым нарушениям пассажа пищи и снижению качества жизни
ВВЕДЕНИЕ
Ахалазия кардии (АК) — относительно редко встречающееся заболевание (10 случаев на 100 тыс. населения) [1], приводящее к значительному снижению качества жизни пациентов [2]. Ахалазия кардии проявляется местными симптомами, такими как дисфагия, боль за грудиной, регургитация пищи, а также снижением массы тела вследствие уменьшения объема принимаемой пищи [3]. Доля пациентов с ахалазией кардии последней, IV стадии, оценивается в 5 % от общего количества больных. АК IV стадии характеризуется значительным (более 6 см) расширением и S образным искривлением пищевода, выявляемым при рентгенографии с контрастом [3–7].
Общепринятым методом хирургического лечения АК на данный момент является эзофагокардиомиотомия.
Особое внимание требуется пациентам в последней, IV стадии АК. Значительное растяжение стенки и S образное искривление пищевода сами по себе представляют помеху для прохождения пищи, даже при устранении сужения в зоне пищеводно-желудочного перехода. Возможно, из-за этого во многих исследованиях и национальных рекомендациях при IV стадии АК рекомендуется использовать более радикальный метод — экстирпацию пищевода [8–10].
Экстирпация с созданием искусственного пищевода из частей пищеварительного тракта пациента характеризуется интраоперационной летальностью около 2 %, симптомы сохраняющегося стеноза в зоне пищеводно-желудочного перехода отмечаются у 1/4 пациентов. До 1/3 пациентов отмечают сохраняющееся снижение качества жизни в отдаленном послеоперационном периоде после экстирпации пищевода [8, 11]. В то же время в последние годы увеличивается количество сообщений об успешном применении органосохраняющих операций при IV стадии АК в виде эзофагокардиомиотомии с различными вариантами противорефлюксных мероприятий: фундопликация по Дор, по Турэ и другие [12]. После подобных операций удавалось достичь сопоставимого качества жизни пациентов по сравнению с экстирпацией пищевода, а интраи послеоперационная летальность при органосохраняющих операциях оказывалась значимо ниже [11, 12].
Анализ опубликованных данных свидетельствует о том, что наиболее частым интраоперационным осложнением при выполнении эзофагокардиомиотомии является повреждение слизистой оболочки пищевода. Средняя частота данного осложнения составляет около 6,9 % и варьирует, по данным разных авторов, в широком диапазоне — от 0 до 33 %.
При этом клинически значимые последствия, сопровождающиеся необходимостью изменения объема оперативного вмешательства, увеличением продолжительности госпитализации или летальным исходом, отмечаются существенно реже — примерно у 0,7 % пациентов (диапазон 0–3 %) [13]. В одном из исследований, включавшем 222 пациента, неудовлетворительный результат миотомии был зафиксирован у 16 больных, что составило 7,2 % наблюдений. Указанное осложнение сопровождалось увеличением продолжительности пребывания в стационаре, однако выраженных неблагоприятных последствий для состояния здоровья пациентов выявлено не было [14].
Основными осложнениями эзофагокардиомиотомии в отдаленном послеоперационном периоде (12–24 месяца и более) являются повторный стеноз в зоне пищеводно-желудочного перехода и гастроэзофагеальный рефлюкс [13, 15]. Тем не менее многие авторы рекомендуют выполнять повторную эзофагокардиомиотомию даже при неэффективности первой операции (оценка симптомов по Eckardt больше 3) [12, 16–18].
Сохранение симптомов ахалазии кардии в отдаленном послеоперационном периоде после эзофагокардиомиотомии может быть обусловлено наличием S образно искривленного пищевода, в нижней части которого пища задерживается даже при проходимости зоны пищеводно-желудочного перехода. Особого внимания заслуживают новые методики, позволяющие выпрямлять вертикальную ось пищевода и улучшить эвакуацию пищи, такие как pull-down Heller-Dor [19], показывающие хорошие результаты в раннем и отдаленном послеоперационном периоде.
Еще одним фактором в выборе методики хирургического лечения АК является наличие или вероятность возникновения злокачественного перерождения эпителия пищевода — в изначальном состоянии ахалазии кардии или при длительном гастроэзофагеальном рефлюксе, возникающем как осложнения эзофагокардиомиотомии. При наличии эндоскопического и гистологического подтверждения — выбор экстирпации пищевода является безальтернативным.
Однако риск возникновения рака пищевода или пищевода Барретта (как предракового состояния) при АК до и после эзофагокардиомиотомии во многих исследованиях оценивается как низкий [20], и снижение качества жизни вследствие экстирпации пищевода, возможно, будет чрезмерным. Исходя из вышеизложенного мы убеждены, что у пациентов с ахалазией кардии IV стадии предпочтительнее предлагать и выполнять органосохраняющую операцию (эзофагокардиомиотомию), а для улучшения результатов использовать технические приемы, способствующие выпрямлению вертикальной оси пищевода. Актуальность исследования заключается в том, что по результатам современных исследований органосохраняющие операции как альтернатива экстирпации пищевода рекомендуются к использованию при ахалазии кардии IV стадии.
На данный момент не существует результатов исследований, предоставляющих убедительные доказательства преимуществ каждого из этих методов и не достигнут консенсус в вопросе выбора метода хирургического лечения, решение о выборе в данный момент остается на усмотрение хирурга. Мы как сторонники сохранения собственного пищевода пациента решили для подтверждения жизнеспособности метода Геллера — Готтштейна провести оценку результатов хирургического лечения с применением способа по выпрямлению вертикальной оси пищевода.
С целью проверки обоснованности указанной позиции был выполнен сравнительный анализ результатов эзофагокардиомиотомии у больных с IV стадией ахалазии кардии, прооперированных с применением классической методики Геллера — Готтштейна, а также ее модифицированного варианта, предусматривающего коррекцию вертикальной оси пищевода.
Цель настоящего исследования — провести сравнительную оценку эффективности эзофагокардиомиотомии у пациентов с ахалазией кардии IV стадии при использовании классической методики и модифицированного подхода, предусматривающего коррекцию вертикальной оси пищевода.
Задачи исследования:
1. Провести сравнительный анализ показателей состояния и качества жизни пациентов с ахалазией кардии IV стадии в исследуемых группах до операции.
2. Провести сравнительный анализ показателей состояния пациентов и осложнений в исследуемых группах в периоперационном периоде.
3. Провести сравнительный анализ показателей состояния и качества жизни пациентов с ахалазией кардии IV стадии в исследуемых группах в отдаленном периоде.
МАТЕРИАЛЫ И МЕТОДЫ
Работа основана на ретроспективном анализе данных хирургического лечения 63 пациентов с установленной IV стадией ахалазии кардии, оперированных в условиях отделения торакальной хирургии ГОБУЗ «Новгородская областная клиническая больница» в период с 1982 по 2024 г. Статистическая обработка и аналитическая интерпретация клинических данных проводились на базе кафедры госпитальной хирургии ФГБОУ ВО «Новгородский государственный университет имени Ярослава Мудрого».
Исследуемую когорту составили пациенты мужского и женского пола в возрастном диапазоне от 20 до 77 лет с клинически подтвержденной ахалазией кардии IV стадии.
Критерием обязательного включения являлось наличие двух контрольных этапов наблюдения: в раннем послеоперационном периоде и спустя 24 месяца после проведенного хирургического лечения. Допускалось наличие сопутствующих заболеваний легкой степени тяжести. Все пациенты предоставили добровольное письменное информированное согласие на участие в исследовании.
Критериями исключения из исследования являлись: пациенты, отказавшиеся от участия, допустившие несоблюдение лечебного и/или исследовательского протоколов, имеющие тяжелые сопутствующие заболевания, а также больные с ахалазией кардии I, II или III стадии. Пациенты были разделены на две группы. В I группу вошли пациенты, прооперированные в 1982–2007 годах, во II группу — прооперированные в 2008–2024 годах.
Пациентам I группы проводилось хирургическое лечение с применением операции Геллера в модификации Готтштейна, включающей внеслизистую эзофагокардиомиотомию с пластикой пищевода передней стенкой желудка, которая использовалась в период с 1982 по 1991 год. В последующем, в 1992–2007 гг., в данной группе применялась разработанная и усовершенствованная авторами модификация операции Геллера — Готтштейна [21].
Пациентам II группы хирургическое лечение осуществлялось с применением операции Геллера — Готтштейна, включающей внеслизистую эзофагокардиомиотомию с пластикой пищевода передней стенкой желудка, дополненной использованием запатентованного способа коррекции вертикальной оси пищевода [21, 22]. В ходе оперативного вмешательства использовалась модифицированная техника по сравнению с традиционной методикой Геллера — Готтштейна.
Рассечение мышечной оболочки выполнялось со стороны левой стенки пищевода с продлением разреза каудально на желудок, формируя миотомию общей протяженностью порядка 11–13 см. Длина разреза кардиального отдела желудка составляла 2–3 см, а при поперечном сшивании формировался острый угол Гиса, что способствовало расширению стенозированного участка и снижению риска гастроэзофагеального рефлюкса. На следующем этапе на мышечную оболочку правой стенки искривленного пищевода накладывались три ряда параллельно расположенных гофрирующих швов с интервалом между ними 0,4–0,8 см и длиной стежков 0,5–0,6 см. Последовательное затягивание и завязывание наложенных лигатур приводило к формированию гофрирования стенки пищевода, восстановлению прямолинейности его вертикальной оси и устранению патологического изгиба (рис. 1).
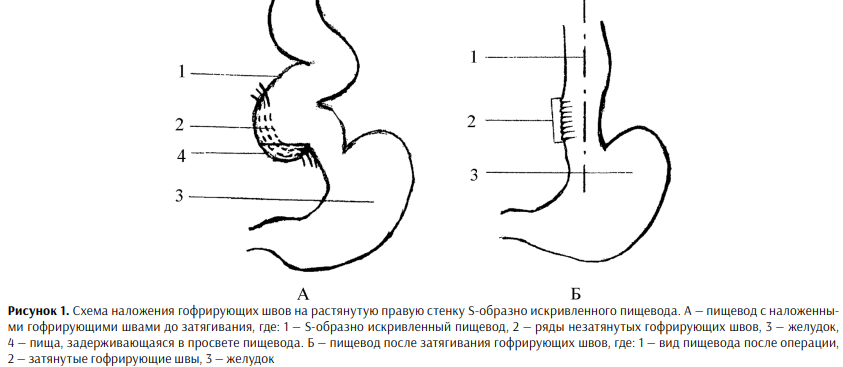
В предоперационном периоде всем пациентам проводилась коррекция алиментарных нарушений. Наблюдение за пациентами осуществлялось поэтапно и включало анализ клинического состояния в раннем послеоперационном периоде (до 5 суток), а также проведение отсроченного контрольного обследования через 24 месяца после операции.

В ближайшие сроки после вмешательства эффективность лечения оценивалась с учетом клинической симптоматики, результатов эндоскопического и рентгенологического исследований с контрастированием, параллельно фиксировались частота ранних осложнений и показатели интра- и послеоперационной летальности. До операции и при контрольном обследовании через 24 месяца степень выраженности клинических проявлений ахалазии кардии определялась пациентами самостоятельно с использованием шкалы Eckardt (табл. 1), предусматривающей суммарную оценку от 0 до 12 баллов [10, 23], а также общий уровень качества жизни, оцениваемый с использованием опросника GIQLI с возможным диапазоном значений от 0 до 144 баллов [24].
Критерием благоприятного исхода оперативного лечения служило одновременное достижение низкой симптоматической нагрузки по шкале Eckardt (не более 3 баллов) и высокого интегрального показателя качества жизни, оцениваемого с использованием опросника GIQLI (более 120 баллов) [25]. В отдаленные сроки после хирургического вмешательства проводилось длительное динамическое наблюдение за пациентами. Материалы, отражающие клиническое состояние и жалобы больных в период, предшествующий применению шкал Eckardt и GIQLI, первоначально фиксировались без использования количественных критериев и впоследствии были ретроспективно трансформированы в стандартизированные показатели для последующего анализа. Максимальная продолжительность наблюдения составила 21 год в I группе и 14 лет во II группе.
Через 24 месяца после оперативного вмешательства контрольное обследование было выполнено у 21 пациента I группы и у 20 пациентов II группы, что соответствовало 60 и 71,4 % от исходного числа наблюдений соответственно.
Обработка и анализ статистических данных осуществлялись с применением программ Microsoft Office 2016 и IBM SPSS Statistics (версия 26). Количественные параметры представлены в формате медианы с указанием межквартильного интервала. Для оценки различий количественных показателей между сравниваемыми группами использовался непараметрический U критерий Манна — Уитни. Сравнение частоты встречаемости качественных признаков проводилось с использованием критерия χ² Фишера. Критическим уровнем статистической значимости при проверке гипотез считалось значение p = 0,05.
РЕЗУЛЬТАТЫ
До операции
Из таблицы 2 видно, что группы сопоставимы по полу, возрасту и длительности заболевания. В предоперационном периоде пациенты отмечали снижение массы тела, постоянную дисфагию, загрудинные боли и регургитацию пищевых масс. Характерным клиническим проявлением являлась парадоксальная дисфагия, при которой прием жидкой пищи сопровождался большими затруднениями по сравнению с твердой.

Жалобы на изжогу у пациентов обеих групп отсутствовали. Оценка выраженности симптомов АК до операции представлена в таблице 3.
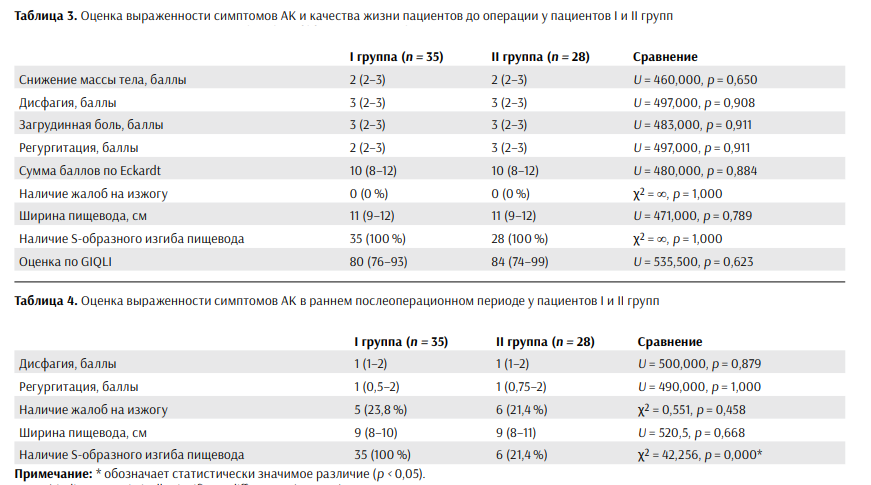
По данным рентгеноскопии с контрастированием водным раствором сульфата бария выявленные изменения соответствовали ахалазии кардии IV стадии согласно классификации Б. В. Петровского [26]. Рентгенологически в нижней трети пищевода отмечалось значительное расширение его просвета: у пациентов I группы медианный диаметр составлял 11 (9–12) см с максимальным значением до 14 см; во II группе показатели были сопоставимыми — 11 (9–12) см, максимальное расширение также достигало 14 см. Во всех наблюдениях регистрировалась S образная деформация пищевода, являющаяся характерным признаком IV стадии ахалазии кардии. Пищевод находился в состоянии атонии, просвет кардии был резко сужен, при этом контрастное вещество задерживалось на срок 2 суток и более.
При эндоскопическом исследовании у всех пациентов выявлялись изменения, характерные для ахалазии кардии IV стадии [27]. Эндоскопическое исследование у всех пациентов выполнялось натощак. Просвет пищевода был расширен до 6–10 см и содержал значительное количество непереваренных пищевых масс и слизи. Слизистая оболочка характеризовалась рыхлостью и утолщением с выраженной поперечной складчатостью; пищевод имел сигмовидную деформацию. Кардиальный сфинктер смыкался неполно, был смещен, при этом на слизистой оболочке выявлялись рубцовые изменения.
Общая оценка качества жизни пациентов по шкале GIQLI составила 80 (76–93) баллов у пациентов I группы и 84 (74– 99) балла у пациентов II группы (между группами U = 535,5, p = 0,623).
Возрастно-половой состав, длительность заболевания, симптомы и результаты инструментальных методов исследования, а также самооценка качества жизни пациентов I и II групп достоверно не отличались (p > 0,05 по всем показателям).
Операция
Средняя продолжительность оперативного вмешательства у пациентов I группы составила 76 (64–88) минут, медианный объем интраоперационной кровопотери — 56 (50–63) мл. Летальных исходов в данной группе не зарегистрировано. В структуре интраоперационных осложнений отмечалась точечная перфорация слизистой оболочки пищевода размером не более 1–1,5 мм, выявленная у 2 пациентов (5,7 %). У пациентов II группы средняя продолжительность оперативного вмешательства составила 85 (76–94) минут, медианный объем интраоперационной кровопотери — 63 (55–74) мл. Летальных исходов в данной группе также не отмечено.
В качестве интраоперационного осложнения зарегистрирован один случай микроперфорации слизистой оболочки пищевода размером 2×1 мм, что составило 3,6 %. Во 2-й группе медиана длительности операции была на 9 мин (11,8 %) больше (U = 670,500, p = 0,013). Медиана объема кровопотери во 2-й группе составляла на 7 мл (12,5 %) больше (U = 651,500, p = 0,025). Частота встречаемости интраоперационных осложнений между группами I и II достоверно не отличалась (χ² = 0,157, p = 0,691).
Ранний послеоперационный период
В раннем послеоперационном периоде все пациенты указывали на полное прекращение постоянной дисфагии, ранее возникавшей при каждом акте глотания. Применение шкал Eckardt и GIQLI в указанные сроки не проводилось, так как данные методы оценки ориентированы на анализ симптоматики в динамике за несколько месяцев.
Дополнительным ограничением являлась невозможность достоверной оценки загрудинной боли вследствие вероятного влияния послеоперационного болевого синдрома в зоне хирургического вмешательства. Оценка выраженности симптомов АК в раннем послеоперационном периоде представлена в таблице 4. После операции у 5 пациентов (23,8 %) I группы и у 6 пациентов (21,4 %) II группы появились жалобы на изжогу (χ² = 0,551, p = 0,458). По данным рентгеноскопии с контрастированием, выполненной через 5 суток после оперативного вмешательства, ширина пищевода у пациентов I группы составила 9 (8–10) см, во II группе — 9 (8–11) см.
Статистически значимых различий между группами выявлено не было (U критерий Манна — Уитни: U = 520,5; p = 0,668).
S образный изгиб пищевода продолжал наблюдаться у 35 (100 %) пациентов. Спустя 24 месяца после операции При контрольном обследовании через 24 месяца после оперативного вмешательства пациенты I группы отмечали эпизодически возникающие (примерно один раз в неделю) симптомы дисфагии у 16 больных (81 %), загрудинной боли — у 12 (57 %) и регургитации — у 13 пациентов (62 %). Жалобы на изжогу в отдаленном послеоперационном периоде появились у 6 пациентов данной группы, что составило 28,6 %. Во II группе эпизодическая дисфагия регистрировалась у 10 пациентов (50 %), загрудинная боль — у 12 (57 %), регургитация — у 4 больных (20,0 %). Симптомы изжоги отмечали 6 пациентов, что соответствовало 30,0 % наблюдений. У всех пациентов обеих групп в отдаленном послеоперационном периоде отмечалось восстановление массы тела до конституциональной нормы. При анализе отдаленных результатов лечения через 24 месяца было установлено, что суммарный балл по шкале Eckardt у пациентов I группы соответствовал значению 3 (1–4), в то время как у пациентов II группы данный показатель был ниже и составлял 2 (0–2,25). Выявленные различия между исследуемыми группами достигали уровня статистической значимости (U = 134,50, p = 0,044). Оценка выраженности симптомов АК спустя 24 месяца после операции представлена в таблице 5.
По данным контрольной рентгеноскопии S образная деформация пищевода в отдаленном периоде сохранялась у 12 пациентов I группы, что составило 34,3 %, тогда как во II группе данный признак выявлялся лишь у одного пациента (5 %). Межгрупповые различия были статистически значимыми (χ² = 18,997; p = 0,000). Медианная ширина пищевода у пациентов I группы составляла 4 (3–5) см, при максимальном зарегистрированном значении 5 см. Во II группе данный показатель был ниже и равнялся 3 (2–3) см, при этом максимальное значение также достигало 5 см. Различия между группами по ширине пищевода носили статистически значимый характер (U критерий Манна — Уитни: U = 123,0; p = 0,018). У всех обследованных пациентов контрастное вещество свободно проходило через кардиальный отдел пищевода. Эндоскопически у 2 (9,5 %) пациентов I группы отмечалась дилатация пищевода максимально до 6 сантиметров, остатки пищи натощак (во II группе случаев расширения более 5 см не отмечено). У 2 пациентов (9,5 %) I группы и у 3 пациентов (15 %) II группы (между группами χ² = 0,287, p = 0,592) наблюдались эндоскопические признаки рефлюкс-эзофагита: гиперемия слизистой, небольшие эрозии над кардиальным сфинктером, занимающие не более 10 % окружности, что соответствует I стадии по Savary — Miller [28]. Оценка качества жизни по шкале GIQLI спустя 24 месяца после операции у пациентов I группы составила 114 (106–129) баллов, у пациентов II группы — 133 (118,75–138,5) балла (критерий Манна — Уитни U = 338,0, p = 0,001).
ОБСУЖДЕНИЕ
До операции у пациентов обеих групп отмечались выраженные симптомы ахалазии кардии: возникающие практически при каждом приеме пищи дисфагия, боль за грудиной, регургитация пищи, а также значительная (более 5–10 кг) потеря массы тела. Жалобы и данные объективных методов обследования (расширение пищевода более 8–10 см и его S образная форма) свидетельствовали о наличии последней, IV стадии ахалазии кардии у всех пациентов, отобранных в I и II группу.
До операции пациенты I и II групп отмечали выраженное снижение качества жизни, до 80 (76–93) и 84 (74–99) баллов по шкале GIQLI соответственно.
Удлинение времени хирургического вмешательства во II группе по сравнению с I группой носило технический характер и было связано с выполнением дополнительной манипуляции — коррекцией конфигурации правой стенки нижней трети пищевода посредством наложения гофрирующих швов, что в среднем увеличивало продолжительность операции на 9 минут. Летальность в обоих группах составила 0 %, интраоперационные осложнения встречались в 5,7 и 3,6 % у пациентов I и II групп соответственно (между группами разница недостоверна), что согласуется с данными других исследователей — 3,1–4,3 % [11, 12]. Следует отметить, что при проведении эзофагоэктомии по поводу последней стадии АК летальность оценивается в 2,0–4,3 %, встречаемость осложнений достигает 30,0–43,8 % [8, 11, 17].
В раннем послеоперационном периоде в обеих группах получены схожие результаты по уменьшению симптомов ахалазии кардии, однако благодаря использованию методики по выпрямлению продольной оси пищевода во II группе удалось добиться исчезновения S образного изгиба у 78,6 % пациентов, хотя достоверной разницы в ширине пищевода между группами не наблюдалось.
Спустя 24 месяца после операции оценка симптомов ахалазии кардии во II группе составляла на 1 балл меньше (p < 0,05), объективно ширина пищевода и встречаемость его S образного изгиба также были достоверно меньше у пациентов II группы.
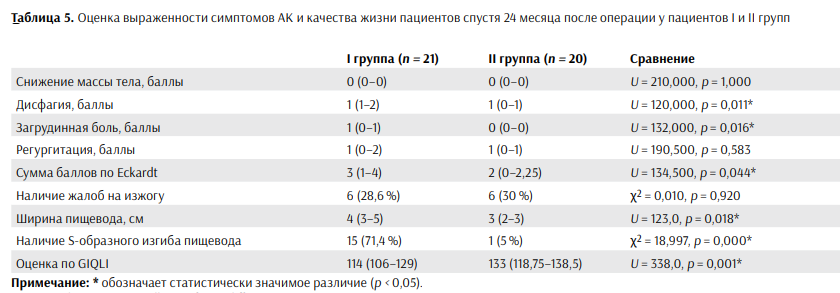
Значимое увеличение качества жизни спустя 24 месяца после операции отметили все пациенты I и II групп. При сравнении между группами достоверно лучший результат отмечался у пациентов II группы (133 против 114 баллов по GIQLI), которым во время операции накладывались гофрирующие швы на правую стенку пищевода в нижней трети для устранения мешкообразного расширения и выпрямления продольной оси. Об эффективности применения методик, направленных на коррекцию S образной деформации пищевода в сочетании с эзофагокардиомиотомией при терминальной стадии ахалазии кардии, сообщается в работах Nezi, Salvador, Tassi и соавт. [11, 12, 19].
За весь период динамического наблюдения, продолжительность которого достигала 40 лет, ни у одного пациента из обеих исследуемых групп не было зафиксировано необходимости в выполнении повторных хирургических вмешательств, включая повторную эзофагокардиомиотомию, баллонную дилатацию либо экстирпацию пищевода. Важно отметить, что хирургические вмешательства на пищеводе в регионе выполняются исключительно в отделении, на базе которого проводилось данное исследование, и случаев необходимости повторных операций за указанный период зарегистрировано
По данным других исследователей, доля пациентов, нуждающихся в повторной операции по поводу АК, может достигать 10–20 % [29]. У пациентов I и II групп, предъявлявших жалобы, характерные для ахалазии кардии, их выраженность соответствовала I–II стадии, и данные жалобы купировались консервативными методами лечения. Следует также отметить, что за весь период наблюдений за пациентами, прооперированными по поводу ахалазии кардии IV стадии (с 1982 года), нам ни разу не встречались злокачественные заболевания пищевода.
Данные других исследователей свидетельствуют о том, что под воздействием желудочного сока эпителий слизистой нижней трети пищевода может претерпевать метаплазию (в частности, пищевод Барретта) [11] и даже малигнизацию [8, 17]. Среди наших пациентов жалобы на изжогу предъявляли 28,6–30 % пациентов, эндоскопические признаки I стадии рефлюкс-эзофагита были выявлены у 9,5– 15 %, без достоверной разницы между группами. Таким образом, исходя из сравнительного анализа мы утверждаем, что применение операции Геллера — Готтштейна в нашей модификации позволяет добиться удовлетворительных результатов при IV стадии АК, и мы считаем, что данный способ может быть рекомендован для внедрения как альтернатива экстирпации пищевода.
ЗАКЛЮЧЕНИЕ
Результаты проведенного исследования показали, что:
1. Пациенты с ахалазией кардии IV стадии предъявляли жалобы на дисфагию, боль за грудиной, регургитацию пищи, потерю массы тела: медиана оценки по Eckardt составляла 10 (8–12) у пациентов обеих групп. Рентгенографическая картина до операции показывала значительное расширение пищевода до 11 (9–12) см и его S образный изгиб у всех пациентов. Свое качество жизни пациенты оценили в 80 (76–93) баллов по GIQLI в I группе и 84 (74–99) балла по GIQLI во II группе. Достоверных различий во всех показателях у пациентов I и II групп до операции обнаружено не было.
2. В раннем послеоперационном периоде все пациенты I и II групп отмечали значительное уменьшение симптомов ахалазии кардии. Рентгенографически, ширина пищевода сократилась до 9 (8–10 см) в I группе пациентов и до 9 (8–11 см) — во II группе (критерий Манна — Уитни U = 520,500, p = 0,668). Частота встречаемости S образного изгиба пищевода в I группе не изменилась, а во II — уменьшилась на 78,6 % (между группами χ² = 42,256, p = 0,000). Следует отметить появление после операции жалоб на изжогу у 5 пациентов (23,8 %) I группы и у 6 пациентов (21,4 %) — II группы (между группами χ² = 0,551, p = 0,458).
3. Спустя 24 месяца после операции оценка симптомов ахалазии кардии по Eckadrt у пациентов II группы была на 1 балл (50 %) меньше, чем у пациентов I группы (U = 134,500, p = 0,044). Ширина пищевода у пациентов II группы также была на 1 см (25 %) меньше (U = 123,000, p = 0,018). Частота встречаемости S образного изгиба пищевода в II группе была значительно меньше: 5 % против 71,4 % у пациентов I группы (χ² = 18,997, p = 0,000). Общая оценка качества жизни по GIQLI у пациентов II группы составила на 19 баллов (16,7 %) больше по сравнению с I группой (U = 338,000, p = 0,001). Жалобы на изжогу встречались у пациентов I группы в 28,6 % случаев, II группы — в 30,0 % (между группами χ² = 0,010, p = 0,920). Признаки I стадии рефлюкс-эзофагита наблюдались у 9,5 % пациентов I и у 15 % II группы (между группами χ² = 0,287, p = 0,592).
СПИСОК ЛИТЕРАТУРЫ
1 Sadowski D.C., Ackah F., Jiang B., Svenson L.W. Achalasia: incidence, prevalence and survival. A population-based study. Neurogastroenterol Motil. 2010;22(9):e256–61. DOI: 10.1111/j.1365-2982.2010.01511.x
2 Slone S., Kumar A., Jacobs J., Velanovich V., Richter J.E. Accuracy of Achalasia Quality of Life and Eckardt scores for assessment of clinical improvement post treatment for achalasia. Dis Esophagus. 2021;34(2):doaa080. DOI: 10.1093/dote/doaa080. PMID: 32875315
3 Savarino E., Bhatia S., Roman S., Sifrim D., Tack J., Thompson S.K., et al. Achalasia. Nat Rev Dis Primers. 2022;8(1):28. DOI: 10.1038/ s41572-022-00356-8
4 Duranceau A., Liberman M., Martin J., Ferraro P. End-stage achalasia. Dis Esophagus. 2012;25(4):319–30. DOI: 10.1111/j.1442- 2050.2010.01157.x
5 Sato H., Fujiyoshi Y., Abe H., Shiwaku H., Shiota J., Sato C., et al. Development of dilated esophagus, sigmoid esophagus, and esophageal diverticulum in patients with achalasia: Japan Achalasia Multicenter Study. J Neurogastroenterol Motil. 2022;28(2):222–30. DOI: 10.5056/jnm21188
6 Pesce M., Pagliaro M., Sarnelli G., Sweis R. Modern achalasia: diagnosis, classification, and treatment. J Neurogastroenterol Motil. 2023;29(4):419–27. DOI: 10.5056/jnm23125
7 Оскретков В.И., Багдасарян Г.И., Андреасян А.Р. Количественная оценка выраженности дисфагии и основных симптомов ахалазии кардии в дооперационном и послеоперационном периодах. Эндоскопическая хирургия. 2021;27(4):17–22. DOI: 10.17116/endoskop20212704117 Oskretkov V.I., Bagdasaryan G.I., Andreasyan A.R. Quantification of dysphagia severity and the main symptoms of cardia achalasia in the preoperative and postoperative periods. Endoscopic Surgery. 2021;27(4):17–22 (In Russ.). DOI: 10.17116/endoskop20212704117
8 Aiolfi A., Asti E., Bonitta G., Siboni S., Bonavina L. Esophageal resection for end-stage achalasia. Am Surg. 2018;84(4):506–11. PMID: 29712597
9 Ручкин Д.В., Оконская Д.Е., Раевская М.Б., Щеголькова Т.А., Арутюнян Н.Э., Глотов А.В. Результаты радикального хирургического лечения ахалазии кардии терминальной стадии. Высокотехнологическая медицина. 2020;7(1):17–31. Ruchkin D.V., Okonskaya D.E., Raevskaya M.B., Shсhegolkova T.A., Arutyunyan N.E., Glotov A.V. Results of radical surgical treatment for end-stage achalasia. Visokotehnologichnaya medicina. 2020;7(1):17–31 (In Russ.).
10 Ивашкин В.Т., Трухманов А.С., Годжелло Э.А., Маев И.В., Евсютина Ю.В., Лапина Т.Л. и др. Рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению ахалазии кардии и кардиоспазма. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2016;26(4):36–54. DOI: 10.22416/1382-4376-2016-4-36-54 Ivashkin V.T., Trukhmanov A.S., Godzhello E.A., Mayev I.V., Evsyutina Yu.V., Lapina T.L., Storonova O.A. Diagnostics and treatment of cardiac achalasia and cardiospasm: guidelines of the Russian gastroenterological association. Russian Journal of Gastroenterology, Hepatology, Coloproctology. 2016;26(4):36–54 (In Russ.). DOI: 10.22416/1382-4376-2016-4-36-54 Rushan A. Sulimanov, Elena Yu. Shestakova, Ramil R. Sulimanov, Egor E. Rumyantsev, Anna A. Sulimanova, Anton S. Chernykh, Olga S. Chernykh Comparative Analysis of Heller–Gottstein Myotomy Outcomes before and after Implementation of a Technique for Straightening the Vertical Axis... Creative Surgery and Oncology 2026;16(1) 13
11 Tassi V., Lugaresi M., Mattioli B., Daddi N., Pilotti V., Ferruzzi L., et al. Quality of life after operation for end-stage achalasia: pulldown Heller-Dor versus esophagectomy. Ann Thorac Surg. 2022;113(1):271–8.
12 Salvador R., Nezi G., Forattini F., Riccio F., Vittori A., Provenzano L., et al. Laparoscopic Heller-Dor is an effective long-term treatment for end-stage achalasia. Surg Endosc. 2023;37(3):1742–8. DOI: 10.1007/s00464-022-09696-8
13 Campos G.M., Vittinghoff E., Rabl C., Takata M., Gadenstätter M., Lin F., et al. Endoscopic and surgical treatments for achalasia: a systematic review and meta-analysis. Ann Surg. 2009;249(1):45–57.
14 Rakita S., Bloomston M., Villadolid D., Thometz D., Boe B., Rosemurgy A. Age affects presenting symptoms of achalasia and outcomes after myotomy. Am Surg. 2005;71(5):424–9. PMID: 15986975
15 Fukushima N., Masuda T., Yano F., Omura N., Tsuboi K., Hoshino M., et al. Over ten-year outcomes of laparoscopic Heller-myotomy with Dor-fundoplication with achalasia: single-center experience with annual endoscopic surveillance. Surg Endosc. 2021;35(12):6513–23. DOI: 10.1007/s00464-020-08148-5
16 Laurino-Neto R.M., Herbella F., Schlottmann F., Patti M. Evaluation of esophageal achalasia: from symptoms to the chicago classification. Arq Bras Cir Dig. 2018;31(2):e1376. DOI: 10.1590/0102-672020180001e1376
17 Felix V.N., Murayama K.M., Bonavina L., Park M.I. Achalasia: what to do in the face of failures of Heller myotomy. Ann N Y Acad Sci. 2020;1481(1):236–46. DOI: 10.1111/nyas.14440
18 Barron J.O., Toth A.J., Blackstone E.H., Ramji S., Jain N., Tasnim S., et al. Heller myotomy for esophageal achalasia: Outcomes in 1010 patients with longitudinal follow-up. J Thorac Cardiovasc Surg. 2025;170(6):1821–30.e4. DOI: 10.1016/j.jtcvs.2025.06.011
19 Nezi G., Forattini F., Provenzano L., Capovilla G., Vittori A., Nicoletti L., et al. The esophageal pull-down technique improves the outcome of laparoscopic Heller-Dor myotomy in end-stage achalasia. J Gastrointest Surg. 2024 Feb 9:S1091-255X(24)00151-3. DOI: 10.1016/j.gassur.2024.02.002
20 Torres-Aguilera M., Remes Troche J.M. Achalasia and esophageal cancer: risks and links. Clin Exp Gastroenterol. 2018;11:309–16. DOI: 10.2147/CEG.S141642
21 Сулиманов Р.А., Бондаренко С.В., Новиков В.Д., Сулиманов Р.Р. Непосредственные и отдаленные результаты хирургического лечения ахалазии кардии IV стадии в нашей модификации. Вестник Новгородского государственного университета. 2012;(66):54–7. Sulimanov R.A., Bondarenko S.V., Novikov V.D., Sulimanov R.R. Immediate and remote results of surgical treatment of achalasia of the cardia stage IV in our modification. Vestnik of Novgorod State University. 2012;(66):54–7 (In Russ.).
22 Сулиманов Р.А., Бондаренко С.В., Новиков В.Д., Рабанал К.Ю.Д., Сулиманов Р.Р. Способ хирургической коррекции ахалазии кардии IV стадии: патент Российская Федерация 2474388 C1 от 10.02.2013. Sulimanov R.A., Bondarenko S.V., Novikov V.D., Sulimanov R.R. Method for surgical correction of stage IV oesophageal achalasia: Russian Federation patent 2474388 C1. 2013 February 10 (In Russ.).
23 Eckardt V.F., Aignherr C., Bernhard G. Predictors of outcome in patients with achalasia treated by pneumatic dilation. Gastroenterology. 1992;103(6):1732–8. DOI: 10.1016/0016-5085(92)91428-7
24 Чикинев Ю.В., Дробязгин Е.А., Судовых И.Е. Качество жизни пациентов после эзофагогастро- и эзофагоколопластики. Вестник экспериментальной и клинической хирургии. 2013;6(1):19–24. Chikinev Iu.V., Drobyazgin E.A., Sudovykh I.E. Quality of Life of Patients and after Esophagogastro- and Esophagocoloplasty. Journal of Experimental and Clinical Surgery. 2013;6(1):19–24 (In Russ.).
25 Цеймах Е.А., Ганков В.А., Багдасарян Г.И., Андреасян А.Р., Масликова С.А. Оценка качества жизни пациентов с ахалазией кардии после видеоэндоскопической кардиомиотомии по Геллеру с фундопликацией по Дору. Acta Biomedica Scientifica. 2022;7(2):272–81. DOI: 10.29413/ABS.2022-7.2.27 Tseymakh E.A., Gankov V.A., Bagdasaryan G.I., Andreasyan A.R., Maslikova S.A. Assessment of the quality of life of patients with achalasia of the cardia after videoendoscopic Heller cardiomyotomy with Dor fundoplication. Acta biomedica scientifica. 2022;7(2):272–81 (In Russ.). DOI: 10.29413/ABS.2022-7.2.27
26 Петровский Б.В. Кардиоспазм и его хирургическое лечение. Труды 27-го Всесоюзного съезда хирургов. М.; 1962. С. 162–73. Petrovsky B.V. Cardiospasm and its surgical treatment. In: Proceedings of the 27th All-Union Congress of Surgeons. Moscow; 1962. Р. 162–73. (In Russ.).
27 Карпов О.Э., Ветшев П.С., Васильев И.В., Маады А.С., Алексеев К.И., Осипов А.С. Эндоскопические технологии в диагностике и лечении ахалазии кардии. Вестник Национального медико-хирургического центра им. НИ Пирогова. 2016;11(1):30–6. Karpov O.Je., Vetshev P.S., VasilYev I.V., Maady A.S., Alekseev K.I., Osipov A.S. Endoscopic techniques in the diagnosis and treatment of achalasia cardii. Bulletin of Pirogov National Medical & Surgical Center. 2016;11(1):30–6 (In Russ.).
28 Оскретков В. И., Григорян М. А., Андреасян А. Р. Алгоритм диагностики рецидива гастроэзофагеальной рефлюксной болезни у больных грыжей пищеводного отверстия диафрагмы после видеолапароскопического антирефлюксного вмешательства. Альманах Института хирургии им. АВ Вишневского. 2022;1:81. Oskretkov V.I., Grigoryan M.A., Andreasyan A.R. Algorithm for diagnosing recurrence of gastroesophageal reflux disease in patients with hiatal hernia after videolaparoscopic antireflux surgery. Almanac of the A.V. Vishnevsky Institute of Surgery. 2022;1:81 (In Russ.). 29 Felix V.N. Esophagectomy for end-stage achalasia. Ann NY Acad Sci. 2016;1381(1):92–7.
Авторы:
Сулиманов Рушан Абдулхакович — д.м.н., профессор, кафедра госпитальной хирургии
Шестакова Елена Юрьевна — кафедра госпитальной хирургии
Сулиманов Рамиль Рушанович — к.м.н., кафедра госпитальной хирургии
Румянцев Егор Евгеньевич — кафедра общей патологии
Сулиманова Анна Амбарцумовна — аспирант, кафедра госпитальной хирургии
Черных Антон Сергеевич — аспирант, кафедра госпитальной хирургии
Черных Ольга Сергеевна — ординатор, кафедра госпитальной хирургии
Теги: пищевод
234567 Начало активности (дата): 07.05.2026
234567 Кем создан (ID): 989
234567 Ключевые слова: ахалазия кардии IV стадии, коррекция вертикальной оси пищевода, эзофагокардиомиотомия, качество жизни, периоперационный период, отдаленные результаты, гастроэзофагеальный рефлюкс
12354567899
Похожие статьи
Грудной желудокРентген на дому 8 495 22 555 6 8
Курс медицинской рентгенологии.Рентгенологическое исследование органов пищеварения (пищевода, желудка, кишечника, желчного аппарата) и диафрагмы.Часть 2. Глава 9.10
Курс медицинской рентгенологии.Рентгенологическое исследование органов пищеварения (пищевода, желудка, кишечника, желчного аппарата) и диафрагмы.Часть 2. Глава 9.9
Курс медицинской рентгенологии.Рентгенологическое исследование органов пищеварения (пищевода, желудка, кишечника, желчного аппарата) и диафрагмы.Часть 2. Глава 9.8



