 14.03.2026
14.03.2026
Влияние бариатрических операций на результаты тотального эндопротезирования при коксартрозе
Бариатрические операции позволяют эффективно лечить морбидное ожирение, которое часто бывает у пациентов с коксартрозом, однако насколько снижение веса после бариатрической хирургии влияет на результаты и частоту осложнений при тотальном эндопротезировании тазобедренного сустава (ТЭТС) изучено недостаточно
ВВЕДЕНИЕ
Ожирение — хроническое заболевание, распространённость которого во всём мире растёт [1]. Люди с ожирением, с индексом массы тела (ИМТ) > 30 кг/м2 , имеют значительно более высокий риск развития остеоартроза (ОА) нижних конечностей [2] из-за увеличения нагрузки и воспалительных адипокинов [3–7]. В сочетании со старением населения рост ожирения, несомненно, приведёт к росту остеоартрита и увеличению спроса на тотальную артропластику суставов. Ежегодно в Соединенных Штатах выполняют более миллиона операций тотального эндопротезирования тазобедренного (ТЭТС) и коленного (TЭKС) суставов [8].
В настоящее время отсутствует консенсус относительно тактики предоперационного ведения пациентов с ожирением и остеоартритом тазобедренного и коленного суставов [9–14]. У этих пациентов более высокий риск послеоперационных осложнений, таких как инфекции, вывихи и ранние ревизии [13, 15–19]. На результаты TЭТС влияют многие факторы, например, местный фактор толщины жирового слоя или окружности верхней трети бедра увеличивает риск вывихов эндопротеза [20], другие факторы оказывают общее влияние на результаты операции. Бариатрическая операция (БО) может положительно воздействовать на некоторые из этих факторов за счет эффекта потери веса, снижает риск от сопутствующих заболеваний, связанных с ожирением, таких как диабет, гипертония и дислипидемия [21–23].
Цель работы — определение влияния бариатрических операций на результаты тотального эндопротезирования тазобедренного сустава и функционального восстановления нижних конечностей с точки зрения наименьшего риска послеоперационных осложнений.
Результаты нескольких научных исследований показали, что пациентам с ожирением и ОА лучше выполнять БО до ТЭТС, потому что это приводит к снижению послеоперационных осложнений [24–26] и боли в тазобедренном суставе, улучшению функциональных результатов [27]. Однако остается нерешенным вопрос оптимального баланса между преимуществами потери веса, с одной стороны, и наименьшим риском ортопедических осложнений, с другой стороны.
МАТЕРИАЛЫ И МЕТОДЫ
В клинике ортопедии и патологии суставов Сеченовского Университета проведено ретроспективнопроспективное когортное одноцентровое контролируемое исследование (одобрено ЛЭК Сеченовского Университета от 14.03.2024 № 06–24).
Мы отобрали основную группу пациентов (n = 62) с коксартрозом 3–4 ст. по классификации K&L (I. Kellgren и I. Lawrence, 1957), направленных в течение пяти лет (с 01.01.2014 по 01.01.2019) для тотального эндопротезирования тазобедренного сустава, имевших в анамнезе морбидное ожирение (ИМТ > 40 кг/м2 ), которым на момент включения в исследование была выполнена БО. В группу сравнения (n = 91) включены пациенты с коксартрозом и морбидным ожирением, сходные по полу и возрасту.
Критерии включения:
— пациенты вне зависимости от пола и возраста с идиопатическим остеоартрозом тазобедренного сустава, характеризующимся болевым синдромом выше 3 баллов по ВАШ, клинико-рентгенологическими признаками 3–4 степени тяжести по классификации К&L, имевшие в анамнезе морбидное ожирение (ИМТ > 40 кг/м2 ), которым перед ТЭТС выполнена БО, подтверждённая медицинской документацией.
— наличие письменного информированного согласия пациента на обработку данных истории болезни и участия в исследовании.
Критерии невключения в исследование:
— наличие грубых деформаций тазобедренного сустава (вальгус, варус, первичные дефекты костной ткани, дисплазия тазобедренного сустава);
— пациенты, проходившие консервативное лечение ожирения;
— системные аутоиммунные заболевания (ревматизм, заболевания соединительной ткани, системный некротизирующий васкулит), тяжелые некорректируемые формы сахарного диабета (гликозилированный гемоглобин > 9 %), заболевания крови (тромбопения, тромбоцитопения, анемия с Hb < 90 г/л), проведение иммунотерапии и/или лечение кортикостероидами, цитостатиками в течение шести месяцев до включения в исследование.
Критерии исключения из исследования:
— отказ пациента от участия в исследовании;
— отсутствие возможности динамического наблюдения и контроля в течение установленного срока (60 месяцев). 51 Гений ортопедии. 2026;32(1)
В течение пяти лет из исследования было исключено 13 (8,5 %) пациентов: из основной группы — три пациента, из группы сравнения — 10 пациентов.
Окончательному анализу подвергнуто 140 пациентов: основная группа — 59 пациентов, группа сравнения — 81 пациентов, из них было 36 (25,7 %) мужчин и 104 (74,3 %) женщины, средний возраст — (63,2 ± 7,0) лет (от 48 до 72 лет).
Пациентам после проведения обследования, подтверждения диагноза «коксартроз» и показаний к ТЭТС выполнили первичное бесцементное ТЭТС и оценили результаты в течение пяти лет после операции.
Для расчета ИМТ (кг/м2 ) вес и рост пациентов измеряли при осмотре и при опросе по телефону. Рост принимали за постоянную величину, а вес пациент сообщал по самостоятельному взвешиванию. Болевой синдром оценивали по 10-бальной визуально-аналоговой шкале ВАШ [28].
Для выявления рентгенологических признаков патологии тазобедренного сустава были использованы переднезадняя проекция и проекция тазобедренного сустава в положении «лягушки». Остеоартрит оценивали по классификации К&L с помощью рентгенографии, показывающей субхондральный склероз, субхондральные кисты, остеофиты бедренной кости или вертлужной впадины или сужение суставной щели [29].
Для оценки состояния тазобедренного сустава применяли модифицированную шкалу Харриса (мШХ), которая состоит из пунктов, оценивающих боль (максимум 44 балла) и функциональность (максимум 47 баллов), что в сумме дает максимум 91 балл.
Оценку осуществляли при опросе пациента по телефону. Результат умножали на 1,1, чтобы получить максимально возможное количество баллов — 100 [30, 31, 32]. Раздел «Функции» включал вопросы о расстоянии, которое пациент может пройти, о его способности надевать обувь и носки, о его способности пользоваться общественным транспортом, о необходимости использовать трость или костыли, о хромоте, о способности подниматься по лестнице и о способности сидеть на обычном стуле в течение часа [33]. Шкала Харриса, по данным систематического обзора N. Ramisetty et al., является наиболее часто употребляемой при изучении результатов ТЭТС [34].
При клиническом обследовании пациенты характеризовали боли по шкале ВАШ со средним уровнем (2,9 ± 1,1) балла, по мШХ (55,7 ± 10,1) балла.
Сравнительный анализ обследования пациентов по группам представлен в табл. 1.
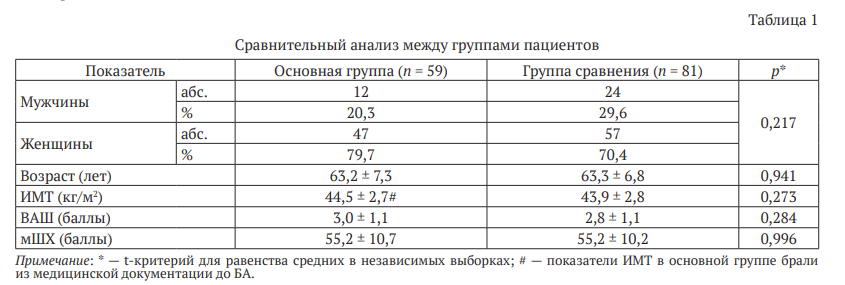
По данным медицинской документации, у пациентов основной группы до БО средний ИМТ составлял (44,5 ± 2,7) кг/м2 , после БО средний ИМТ составил (35,5 ± 2,6) кг/м2 , то есть снижение веса произошло на 20,2 %.
БО у пациентов основной группы, выполненные за (14,2 ± 1,4) мес. до ТЭТС: рукавная резекция желудка — у 44 (74,6 %), межкишечный анастомоз — у 12 (20,3 %), комбинированная операция — у трех (5,1 %) пациентов.
В основную группу исследования вошли пациенты с избыточным весом, 1 и 2 стадиями ожирения (табл. 2).
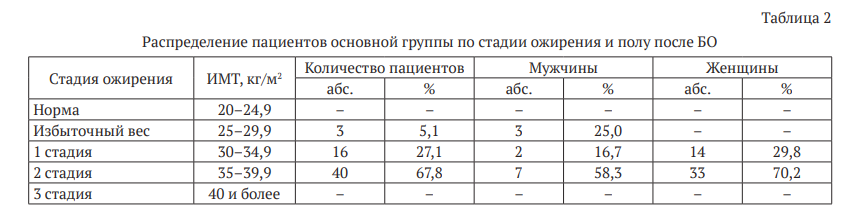
Необходимо отметить, что все пациенты покинули группу морбидного ожирения, но до нормального ИМТ не дошел ни один пациент, только трое мужчин перешли в группу пациентов с избыточным весом, ни одна из женщин не достигла такого результата. Таким образом, основная масса пациентов перешла в группы ожирения 1 и 2 стадий (56 пациентов, 94,9 %).
При опросе многие пациенты утверждали, что их масса тела значительно снижалась до шести месяцев после операции, а затем снова начала нарастать, однако точные достоверные данные нам собрать не удалось.
В послеоперационном периоде мы оценивали следующие показатели: болевой синдром по шкале ВАШ на первые, третьи, седьмые и 14-е сутки; функциональный результат по мШХ через три и 12 месяцев, затем каждые 12 месяцев до 60 месяцев; наличие ранних послеоперационных осложнений в первые три месяца после операции. Далее мы определяли выживаемость эндопротезов и структуру ревизионных операций каждые 12 месяцев до 60 месяцев.
Статистический анализ выполняли с помощью пакета программ IBM SPSS Statistics 22. Взвешенную разность средних значений (WMD) использовали в группе с ожирением при определении ИМТ, для оценки болевого синдрома (ВАШ), баллов по шкале Харриса с соответствующими 95 % ДИ (Cl). Для оценки ранних и поздних осложнений в послеоперационном периоде использовали критерий Манна – Уитни, выживаемости эндопротезов — метод Каплана – Майера.
РЕЗУЛЬТАТЫ
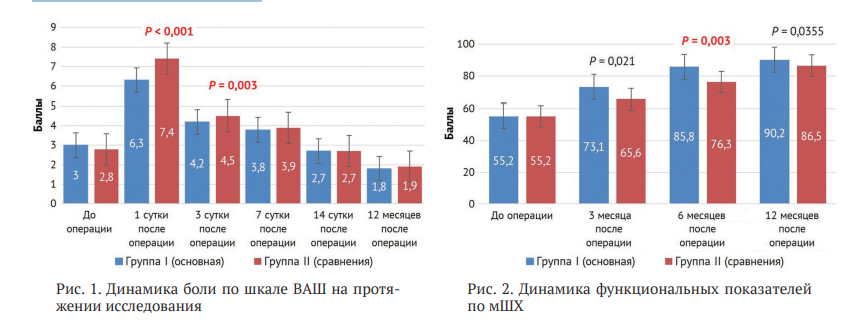
Болевой синдром по шкале ВАШ до операции в группах исследований был на одном уровне и не имел статистически значимой разницы (р < 0,001). На первые сутки после операции показатель резко увеличивался со значительной статистической разницей (р < 0,001). К третьим суткам после операции значения снижались, но разница была статистически значима, р = 0,003. К седьмым и 14-м суткам болевой синдром был купирован, и различия между группами отсутствовали. К окончанию периода наблюдений в 12 месяцев болевой синдром по шкале ВАШ был значительно ниже, чем до операции и статистической разницы результатов между группами не выявлено, р = 0,243 (рис. 1). Результаты тестирования пациентов по модифицированной шкале Харриса до операции в обеих группах были одинаковыми, р = 0,364. После операции показатели функции тазобедренного сустава постепенно прогрессивно увеличиваются со статистически значимой разницей к трем месяцам р = 0,021, к шести месяцам р = 0,003, к 12 месяцам достигают максимума при статистически значимой разнице результатов р = 0,021 (рис. 2).
При анализе выживаемости (отсутствие осложнений) в течение пяти лет после операции (60 месяцев) по методу Каплана – Майера мы получили пятилетнюю выживаемость эндопротезов в основной группе исследования 94,6 % (5,4 % осложнений), в группе сравнения 77,2 % (22,8 % осложнений). На основании этого можно заключить, что применение БО у пациентов с коксартрозом 3–4 ст. по классификации K&L обеспечивает снижение риска осложнений на 17,4 % (Log Rank (Mantel-Cox) р = 0,006), что представлено на рис. 3.
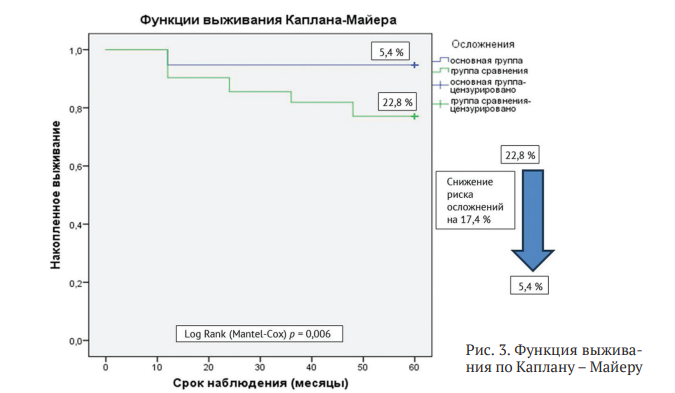
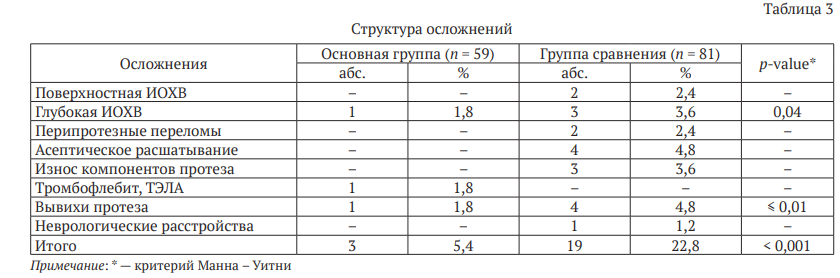
При детальном анализе осложнений мы выявили, что поверхностные инфекции в области хирургического вмешательства у пациентов группы сравнения имели место в 2,4 % случаев и не встретились у пациентов основной группы, а глубокая и перипротезная инфекция у пациентов группы сравнения встречалась в два раза чаще: в основной группе исследования — 1,8 %, в группе сравнения — 3,6 % (табл. 3). Все четыре случая глубокой инфекции и один из двух случаев поверхностной инфекции в нашем исследовании потребовали удаления эндопротеза и двухэтапного ревизионного вмешательства в первые два года исследования. Тромбофлебит глубоких вен голени имел место одном случае у пациента основной группы в раннем послеоперационном периоде (1,8 %), неврит седалищного нерва — в одном случае в группе сравнения (1,2 %), эти осложнения не потребовали ревизионных вмешательств. Перипротезные переломы (2,4 %), асептическое расшатывание (4,8 %) и износ компонентов протеза (3,6 %) в нашем исследовании встретились только у пациентов группы сравнения, причем в последние два года наблюдения, что и определило характер ранних ревизионных операций, не связанных с инфекцией области хирургического вмешательства.
Такие осложнения как вывихи эндопротезов зарегистрированы в обеих группах, однако у пациентов с ИМТ < 40 кг/м2 , которым были выполнены БО, встречались значительно реже: у пациентов основной группы — в 1,8 % случаев (ревизионное вмешательство не потребовалось), в группе сравнения — в 4,8 % случаев (всем выполнили одноэтапные ревизионные оперативные вмешательства).
ОБСУЖДЕНИЕ
Пациенты с ИМТ > 40 кг/м2 имеют относительный риск для TЭТС более чем в 30 раз выше, чем пациенты с ИМТ < 25 кг/м2 [35]. Хирургическое снижение веса является наиболее эффективным средством у пациентов с ожирением, и некоторые авторы указывают, что оно снижает сопутствующие заболевания, связанные с ожирением, и продлевает жизнь [36, 37].
Поскольку существуют ассоциации как между ожирением и риском ОА суставов нижних конечностей, так и между ожирением и осложнениями после TЭТС, важно понять, является ли ожирение модифицируемым фактором риска до ТЭТС. Целью нашего исследования было изучение влияния БО с положительными или отрицательными эффектами на результаты TЭТС. Мы обнаружили, что применение БО у пациентов с коксартрозом 3–4 ст. по классификации K&L обеспечивает снижение риска осложнений на 17,4 %, в частности уменьшает риск послеоперационных инфекционных осложнений, как поверхностных, так и глубоких. Наиболее важным явилось снижение количества ревизионных операций после БО, что подтверждается данными других исследований [38].
В некоторых исследованиях не отмечено увеличение риска повторных операций после БО и последующего ТЭТС [39, 40, 41], в других исследованиях отмечена более высокая частота повторных операций у пациентов с БО и TKA по сравнению с пациентами с низким ИМТ, перенесшими TЭТС [42, 43, 44], только одно исследование показало снижение риска повторной операции TЭТС у пациентов после БО [45].
Исследования, изучающие влияние БО на частоту осложнений в раннем послеоперационном периоде после TЭТС, также дали неоднозначные результаты [38, 39, 42, 46].
Внутрибольничные осложнения могли возникать реже у тех, у кого БО проведена до TЭТС, чем у пациентов с патологическим ожирением [38]. Три исследования [39, 47, 48], включающие 233 пациента, не обнаружили разницы в ранних осложнениях, когда пациенты были стратифицированы по временному интервалу между БО и TЭТС.
Самое крупное исследование, оценивающее влияние БО на ранние осложнения, включавше 5914 пациентов, показало, что осложнения были наиболее частыми у пациентов, у которых были БО до TЭТС. Следует отметить, что потенциальным фактором, мешающим результатам, является то, что предшествующие сопутствующие заболевания также были более частыми в этой группе [38, 42, 45–47, 49–51].
В целом, мы обнаружили, что нет консенсуса, основанного на текущих доказательствах необходимости выполнения БО перед TЭТС, однако каждое исследование следует критически проанализировать. В нескольких сравнительных исследованиях дисбаланс сопутствующих заболеваний в группах исследования мог исказить их анализы и сместить их против когорт БО, поскольку хорошо известно, что пациенты с патологическим ожирением, перенесшие БО, как правило, имеют более высокое исходное количество сопутствующих заболеваний, чем пациенты с патологическим ожирением, не перенесшие БО [52, 53]. Учитывая, что пациенты с ожирением составляют все большую долю пациентов, которым выполняют ТЭТС, оптимизация риска в этой более сложной с медицинской точки зрения популяции пациентов имеет клиническое значение. Пациенты с ожирением чаще испытывают осложнения, включая поверхностную и глубокую инфекцию, острое повреждение почек, остановку сердца и повторную операцию после TЭТС [16, 54]. Ожирение также независимо увеличивает медицинские расходы, связанные с TЭТС [55]. БО оценивается как способ потенциального снижения риска операции у пациентов морбидным ожирением, но, учитывая риски второй плановой операции, крайне важно, чтобы ортопеды давали рекомендации своим пациентам на основе понимания современной литературы. Ни одно исследование не оценивало, устраняет ли снижение веса после БО необходимость в TЭТС. Повышенная подвижность и упражнения после БО могут увеличить количество пациентов, которым требуется в последующем TЭТС [56]. Этот вопрос остается спорным, так как некоторые исследователи предполагают, что уменьшение жалоб пациентов связаны с потерей веса после БО [57].
Необходимы дальнейшие исследования для оценки доли пациентов, которым требуется TЭТС после БО, также было бы полезно сравнить БО с консервативным лечение ожирения перед операцией на тазобедренном суставе, чтобы определить, как отличаются результаты [47]. Наконец, растет популярность проведения рукавной резекции желудка, более выигрышной по сравнению с лапароскопическим шунтированием желудка по Ру [58]. Литературные данные остаются противоречивыми относительно воздействия БО на ранние, краткосрочные и долгосрочные послеоперационные осложнения после TЭТС. В частности, влияние различных типов БО на результаты TЭТС еще предстоит выяснить. В идеале требуются проспективные исследования с более высоким уровнем доказательств, чтобы сделать определенные выводы относительно воздействия БО на результаты TЭТС. Наше исследование продемонстрировало, что очень немногие пациенты теряют вес до проведения операции по замене сустава. Это подчеркивает необходимость целенаправленных нехирургических мероприятий по снижению веса для пациентов, которые в настоящее время ожидают замены сустава.
ЗАКЛЮЧЕНИЕ
Применение бариатрических операций у пациентов с морбидным ожирение и коксартрозом 3–4 ст. перед выполнением ТЭТС позволяет статистически значимо снизить риск послеоперационных осложнений на 17,4 % и повысить пятилетнюю выживаемость эндопротезов до 94,6 %.
СПИСОК ИСТОЧНИКОВ
1. World Health Organization. Obesity and overweight. 2025.
2. Bourne R, Mukhi S, Zhu N, et al. Role of obesity on the risk for total hip or knee arthroplasty. Clin Orthop Relat Res. 2007;465:185-188. doi: 10.1097/BLO.0b013e3181576035.
3. Vuolteenaho K, Koskinen A, Moilanen E. Leptin - a link between obesity and osteoarthritis. applications for prevention and treatment. Basic Clin Pharmacol Toxicol. 2014;114(1):103-108. doi: 10.1111/bcpt.12160.
4. Long H, Xie D, Zeng C, et al. Association between body composition and osteoarthritis: A systematic review and meta-analysis. Int J Rheum Dis. 2019;22(12):2108-2118. doi: 10.1111/1756-185X.13719.
5. Mellion KM, Grover BT. Obesity, Bariatric Surgery, and Hip/Knee Arthroplasty Outcomes. Surg Clin North Am. 2021;101(2):295-305. doi: 10.1016/j.suc.2020.12.011.
6. Sowers MR, Karvonen-Gutierrez CA. The evolving role of obesity in knee osteoarthritis. Curr Opin Rheumatol. 2010;22(5):533-537. doi: 10.1097/BOR.0b013e32833b4682.
7. Francisco V, Pérez T, Pino J, et al. Biomechanics, obesity, and osteoarthritis. The role of adipokines: When the levee breaks. J Orthop Res. 2018;36(2):594-604. doi: 10.1002/jor.23788.
8. Steiner C, Andrews R, Barrett M, Weiss A. HCUP projections: Mobility/orthopedic procedures 2003 to 2012. HCUP projections report # 2012-03. U.S. Agency for Healthcare Research and Quality. 2012.
9. Godziuk K, Prado CM, Beaupre L, et al. A critical review of weight loss recommendations before total knee arthroplasty. Joint Bone Spine. 2021;88(2):105114. doi: 10.1016/j.jbspin.2020.105114.
10. Hooper JM, Deshmukh AJ, Schwarzkopf R. The Role of Bariatric Surgery in the Obese Total Joint Arthroplasty Patient. Orthop Clin North Am. 2018;49(3):297-306. doi: 10.1016/j.ocl.2018.02.003.
11. Stavrakis AI, Khoshbin A, McLawhorn AS, Parks ML. Bariatric Surgery Prior to Total Joint Arthroplasty, Does it Decrease the Risk of Obesity Related Perioperative Complications Curr Rheumatol Rep. 2018;20(2):7.
12. Murr MM, Streiff WJ, Ndindjock R. A Literature Review and Summary Recommendations of the Impact of Bariatric Surgery on Orthopedic Outcomes. Obes Surg. 2021;31(1):394-400. doi: 10.1007/s11695-020-05132-9.
13. Smith TO, Aboelmagd T, Hing CB, MacGregor A. Does bariatric surgery prior to total hip or knee arthroplasty reduce post-operative complications and improve clinical outcomes for obese patients Systematic review and meta-analysis. Bone Joint J. 2016;98- B(9):1160-1166
14. Sherman WF, Patel AH, Kale NN, et al. Surgeon Decision-Making for Individuals With Obesity When Indicating Total Joint Arthroplasty. J Arthroplasty. 2021;36(8):2708-2715.e1. doi: 10.1016/j.arth.2021.02.078.
15. Chen MJ, Bhowmick S, Beseler L, et al. Strategies for Weight Reduction Prior to Total Joint Arthroplasty. J Bone Joint Surg Am. 2018;100(21):1888-1896. doi: 10.2106/JBJS.18.00020.
16. Kerkhoffs GM, Servien E, Dunn W, et al. The influence of obesity on the complication rate and outcome of total knee arthroplasty: a meta-analysis and systematic literature review. J Bone Joint Surg Am. 2012;94(20):1839-1844
17. Wagner ER, Kamath AF, Fruth K, et al. Effect of Body Mass Index on Reoperation and Complications After Total Knee Arthroplasty. J Bone Joint Surg Am. 2016;98(24):2052-2060. doi: 10.2106/JBJS.16.00093.
18. Electricwala AJ, Jethanandani RG, Narkbunnam R, et al. Elevated Body Mass Index Is Associated With Early Total Knee Revision for Infection. J Arthroplasty. 2017;32(1):252-255. doi: 10.1016/j.arth.2016.05.071.
19. Werner BC, Higgins MD, Pehlivan HC, et al. Super Obesity Is an Independent Risk Factor for Complications After Primary Total Hip Arthroplasty. J Arthroplasty. 2017;32(2):402-406. doi: 10.1016/j.arth.2016.08.001.
20. Hernigou P, Trousselier M, Roubineau F, et al. Dual-mobility or Constrained Liners Are More Effective Than Preoperative Bariatric Surgery in Prevention of THA Dislocation. Clin Orthop Relat Res. 2016;474(10):2202-2210.
21. O’Brien PE, Hindle A, Brennan L, et al. Long-Term Outcomes After Bariatric Surgery: a Systematic Review and Meta-analysis of Weight Loss at 10 or More Years for All Bariatric Procedures and a Single-Centre Review of 20-Year Outcomes After Adjustable Gastric Banding. Obes Surg. 2019;29(1):3-14
22. Mingrone G, Panunzi S, De Gaetano A, et al. Bariatric surgery versus conventional medical therapy for type 2 diabetes. N Engl J Med. 2012;366(17):1577-1585. doi: 10.1056/NEJMoa1200111.
23. Sjöström L. Review of the key results from the Swedish Obese Subjects (SOS) trial - a prospective controlled intervention study of bariatric surgery. J Intern Med. 2013;273(3):219-234. doi: 10.1111/joim.12012.
24. Li S, Luo X, Sun H, et al. Does Prior Bariatric Surgery Improve Outcomes Following Total Joint Arthroplasty in the Morbidly Obese? A Meta-Analysis. J Arthroplasty. 2019;34(3):577-585.
25. Gu A, Cohen JS, Malahias MA, et al. The Effect of Bariatric Surgery Prior to Lower-Extremity Total Joint Arthroplasty: A Systematic Review. HSS J. 2019;15(2):190-200. doi: 10.1007/s11420-019-09674-2.
26. Wang Y, Deng Z, Meng J, et al. Impact of Bariatric Surgery on Inpatient Complication, Cost, and Length of Stay Following Total Hip or Knee Arthroplasty. J Arthroplasty. 2019;34(12):2884-2889.e4. doi: 10.1016/j.arth.2019.07.012.
27. Heuts EAF, de Jong LD, Hazebroek EJ, et al. The influence of bariatric surgery on hip and knee joint pain: a systematic review. Surg Obes Relat Dis. 2021;17(9):1637-1653. doi: 10.1016/j.soard.2021.04.019.
28. Huskisson EC. Measurement of pain. Lancet. 1974;2(7889):1127-1131. doi: 10.1016/s0140-6736(74)90884-8.
29. Kellgren, J.H.; Lawrence, J.S. Radiological assessment of osteo-arthrosis. Ann Rheum Dis. 1957;16(4):494-502. doi: 10.1136/ ard.16.4.494.
30. Harris WH. Traumatic arthritis of the hip after dislocation and acetabular fractures: treatment by mold arthroplasty. An end-result study using a new method of result evaluation. J Bone Joint Surg Am. 1969;51(4):737-755.
31. Byrd JW, Jones KS. Hip arthroscopy in the presence of dysplasia. Arthroscopy. 2003;19(10):1055-1060. doi: 10.1016/j. arthro.2003.10.010.
32. Ramisetty N, Kwon Y, Mohtadi N. Patient-reported outcome measures for hip preservation surgery-a systematic review of the literature. J Hip Preserv Surg. 2015;2(1):15-27. doi: 10.1093/jhps/hnv002.
33. Krueger DR, Leopold VJ, Schroeder JH, et al. Correlation of the Subjective Hip Value with Validated Patient-Reported Outcome Measurements for the Hip. J Clin Med. 2020;9(7):2179. doi: 10.3390/jcm9072179.
34. Sato EH, Stevenson KL, Blackburn BE, Peters CL, Archibeck MJ, Pelt CE, Gililland JM, Anderson LA. Impact of Demographic Variables on Recovery After Total Hip Arthroplasty. J Arthroplasty. 2024 Mar;39(3):721-726.
35. Bourne R, Mukhi S, Zhu N, et al. Role of obesity on the risk for total hip or knee arthroplasty. Clin Orthop Relat Res. 2007;465:185-188.
36. Avenell A, Robertson C, Skea Z, et al. Bariatric surgery, lifestyle interventions and orlistat for severe obesity: the REBALANCE mixedmethods systematic review and economic evaluation. Health Technol Assess. 2018;22(68):1-246.
37. Grams J, Garvey WT. Weight Loss and the Prevention and Treatment of Type 2 Diabetes Using Lifestyle Therapy, Pharmacotherapy, and Bariatric Surgery: Mechanisms of Action. Curr Obes Rep. 2015;4(2):287-302.
38. McLawhorn AS, Levack AE, Lee YY, et al. Bariatric Surgery Improves Outcomes After Lower Extremity Arthroplasty in the Morbidly Obese: A Propensity Score-Matched Analysis of a New York Statewide Database. J Arthroplasty. 2018;33(7):2062-2069
39. Kulkarni A, Jameson SS, James P, et al. Does bariatric surgery prior to lower limb joint replacement reduce complications? Surgeon. 2011;9(1):18-21. doi: 10.1016/j.surge.2010.08.004.
40. Nearing EE 2nd, Santos TM, Topolski MS, et al. Benefits of bariatric surgery before elective total joint arthroplasty: is there a role for weight loss optimization? Surg Obes Relat Dis. 2017;13(3):457-462.
41. Slim K, Nini E, Forestier D, et al. Methodological index for non-randomized studies (minors): development and validation of a new instrument. ANZ J Surg. 2003;73(9):712-716. doi: 10.1046/j.1445-2197.2003.02748.x.
42. Lee GC, Ong K, Baykal D, et al. Does Prior Bariatric Surgery Affect Implant Survivorship and Complications Following Primary Total Hip Arthroplasty/Total Knee Arthroplasty? J Arthroplasty. 2018;33(7):2070-2074.e1. doi: 10.1016/j.arth.2018.01.064.
43. Martin JR, Watts CD, Taunton MJ. Bariatric surgery does not improve outcomes in patients undergoing primary total knee arthroplasty. Bone Joint J. 2015;97-B(11):1501-1505. doi: 10.1302/0301-620X.97B11.36477.
44. Odum SM, Springer BD, Dennos AC, Fehring TK. National obesity trends in total knee arthroplasty. J Arthroplasty. 2013;28(8 Suppl):148-151. doi: 10.1016/j.arth.2013.02.036.
45. Werner BC, Kurkis GM, Gwathmey FW, Browne JA. Bariatric Surgery Prior to Total Knee Arthroplasty is Associated With Fewer Postoperative Complications. J Arthroplasty. 2015;30(9 Suppl):81-85. doi: 10.1016/j.arth.2014.11.039.
46. Nickel BT, Klement MR, Penrose CT, et al. Lingering Risk: Bariatric Surgery Before Total Knee Arthroplasty. J Arthroplasty. 2016;31(9 Suppl):207-211. doi: 10.1016/j.arth.2016.02.075.
47. Inacio MC, Paxton EW, Fisher D, et al. Bariatric surgery prior to total joint arthroplasty may not provide dramatic improvements in post-arthroplasty surgical outcomes. J Arthroplasty. 2014;29(7):1359-1364.
48. Nearing EE 2nd, Santos TM, Topolski MS, et al. Benefits of bariatric surgery before elective total joint arthroplasty: is there a role for weight loss optimization Surg Obes Relat Dis. 2017;13(3):457-462.
49. Sturm R. Increases in morbid obesity in the USA: 2000-2005. Public Health. 2007;121(7):492-496. doi: 10.1016/j.puhe.2007.01.006.
50. Schwarzkopf R, Lavery JA, Hooper J, et al. Bariatric Surgery and Time to Total Joint Arthroplasty: Does It Affect Readmission and Complication Rates? Obes Surg. 2018;28(5):1395-1401. doi: 10.1007/s11695-017-3034-6. 51. Severson EP, Singh JA, Browne JA, et al. Total knee arthroplasty in morbidly obese patients treated with bariatric surgery: a comparative study. J Arthroplasty. 2012;27(9):1696-1700.
52. Pontiroli AE, Ceriani V, Sarro G, et al. Incidence of Diabetes Mellitus, Cardiovascular Diseases, and Cancer in Patients Undergoing Malabsorptive Surgery (Biliopancreatic Diversion and Biliointestinal Bypass) vs Medical Treatment. Obes Surg. 2019;29(3):935-942. doi: 10.1007/s11695-018-3601-5.
53. Pories WJ. Bariatric surgery: risks and rewards. J Clin Endocrinol Metab. 2008;93(11 Suppl 1):S89-S96. doi: 10.1210/jc.2008-1641.
54. Ward DT, Metz LN, Horst PK, et al. Complications of Morbid Obesity in Total Joint Arthroplasty: Risk Stratification Based on BMI. J Arthroplasty. 2015;30(9 Suppl):42-46. doi: 10.1016/j.arth.2015.03.045.
55. Kremers HM, Visscher SL, Kremers WK, et al. The effect of obesity on direct medical costs in total knee arthroplasty. J Bone Joint Surg Am. 2014;96(9):718-724.
56. Trofa D, Smith EL, Shah V, Shikora S. Total weight loss associated with increased physical activity after bariatric surgery may increase the need for total joint arthroplasty. Surg Obes Relat Dis. 2014;10(2):335-339.
57. Groen VA, van de Graaf VA, Scholtes VA, Sprague S, van Wagensveld BA, Poolman RW. Effects of bariatric surgery for knee complaints in (morbidly) obese adult patients: a systematic review. Obes Rev. 2015;16(2):161-170.
58. Mechanick JI, Youdim A, Jones DB, et al. Clinical practice guidelines for the perioperative nutritional, metabolic, and nonsurgical support of the bariatric surgery patient--2013 update: cosponsored by American Association of Clinical Endocrinologists, The Obesity Society, and American Society for Metabolic & Bariatric Surgery. Obesity (Silver Spring). 2013;21 Suppl 1(0 1):S1-S27
Информация об авторах:
Андемиркан Олегович Ахов — аспирант
Алексей Владимирович Лычагин — доктор медицинских наук, доцент, заведующий кафедрой
Андрей Анатольевич Грицюк — доктор медицинских наук, профессор, профессор кафедры
Роза Хазбулатовна Явлиева — кандидат медицинских наук, доцент кафедры
Теги: коксартроз
234567 Начало активности (дата): 14.03.2026 06:00:00
234567 Кем создан (ID): 989
234567 Ключевые слова: морбидное ожирение, коксартроз, бариатрические операции
12354567899
Похожие статьи
Методология оценки ходьбы для выявления усталостных и декомпенсаторных механизмов работы опорно-двигательной системы у больных коксартрозомРентген на дому 8 495 22 555 6 8
Современные аспекты в лечении пациентов с коксартрозом
Возможности лечения методом радиочастотной денервации при коксартрозе различных стадий
Влияние предшествовавшего оперативного лечения на результаты тотального эндопротезирования тазобедренного сустава у молодых пациентов с диспластическим коксартрозом



