 12.05.2026
12.05.2026
Выбор способа пластики пролежня области большого вертела бедренной кости у пациентов со спинальной травмой
Проблема лечения пролежней области большого вертела бедренной кости у пациентов с послед ствиями спинальной травмы остается в центре пристального внимания клиницистов и исследователей
Введение.
Пролежневые дефекты области большого вертела являются одними из самых частых и трудно поддающихся лечению. В среднем их количество составляет 20–27 % от всех декубитальных язв, возникающих у пациентов с повреждением спинного мозга [1]. Частота их возникновения об условлена разными причинами, основными среди них являются постоянное положения бедра на боку под углом 90° вместо необходимых 30–40°, наличие выраженного костного выступа в виде большого вертела бедренной кости, который оказывает постоянное давление на покровные ткани выше допустимых 23,7 мм рт. ст. [2]. Близкое расположение суставной поверхности предрасполагает к распространению очага инфекции на глубокие ткани с последующим развитием периостита, остеомиелита, септического артрита и, как следствие, сепсиса, который является основным предиктором летальности пациентов с пролежнями вертельной области (33 %) [3].
Цель исследования – систематизировать литературные данные и на основании данных собственного клинического исследования оценить эффективность различных видов реконструктивно пластических операций, используемых при закрытии пролежня области большого вертела бедренной кости у пациентов со спинальной травмой.
Выбор пластики в первую очередь зависит от размеров пролежневого дефекта, его геометрии, вовлечения в патологический процесс глубже лежащих тканей и имеет свои особенности и правила, несоблюдение которых сопряжено с развитием ряда осложнений, приводящих к рецидивам в 25 % случаев [4]. Таким образом, для снижения рисков развития послеоперационных осложнений, рецидивов пролежней проекции большого верте ла бедренной кости у пациентов с травматической болезнью спинного мозга требуется комплексный анализ возможных реконструктивных методов закрытия пролежней данной локализации.
Методы и материалы.
В базах данных PubMed, Cochrane Library, Science Direct, Google Scholar, eLibrary по ключевым словам «пролежень» или «декубитальная язва» + «большой вертел» или + «реконструкция пролежня» или + «пластика про лежней» или + «осложнения пролежней» проведен поиск статей, опубликованных в 2019–2024 гг. В предварительный анализ включены 1322 источника. Критерии исключения источников из анализа: не описаны результаты хирургического лечения пролежней проекции большого вертела бедренной кости, не представлены методики реконструктивных методик, не указаны осложнения, связанные с тем или иным методом лечения. В итоге про анализированы данные 30 источников, изданных в период последних 5 лет. Из них: 7 метаанализов, 6 РКИ, 6 клинических исследований, 10 литературных обзоров, 1 экспериментальное исследование. Включены 7 источников, опубликованных ранее 5 лет, по причине их фундаментальной и практической значимости для рассматриваемого вопроса. В проспективное исследование включен 61 пациент с пролежнями области большого вертела бедренной кости и получивших оперативное лечение различными способами пластик.
Критерии включения: пациенты с травматической болезнью спинного мозга, имеющие пролежневые дефекты III и IV стадии в области большого вертела бедренной кости, в возрасте от 18 до 59 лет, с периодом после получения травмы не менее одного года.
Критерии исключения: пролежни, локализация которых не распространялась на область большо го вертела бедренной кости и возникшие на фоне других заболеваний, наличие приобретенного им мунодефицита; политравма с повреждением полых, паренхиматозных органов брюшной полости; наличие тяжелой пневмонии в анамнезе; перенесен ная трансплантация костного мозга в анамнезе; наличие таких сопутствующих заболеваний, как сахарный диабет, онкологические заболевания, ХОБЛ, цирроз печени, ХПН, перелом шейки бедра, гемобластоз, перенесенный инсульт.
Результаты.
Анализ литературных данных показал, что лечение декубитальных язв вертельной области в первую очередь требует мультидисциплинарного подхода с привлечением различных узкопрофильных специалистов: дерматолога, физиотерапевта, хирурга, нейрохирурга, травматолога ортопеда, специалиста по хирургической инфекции, реаниматолога, клинического фармаколога, диетолога и ряда других. Консервативные методы, даже с привлечением групп специалистов, распространяются лишь на поверхностные пролежневые дефекты и зачастую являются малоэффективными [5]. Хирургическое вмешательство является основным методом лечения декубитальных язв вертельной области, однако и оно сопряжено с большим количеством осложнений, таких как инфекция раны, которая в среднем варьирует от 35 до 50 %, некроз сформированного лоскута – 12,5 %, а также после операционные гематомы, серомы, ишемия лоскута развиваются с частотой в 17 % и все это, прежде всего, связано с неадекватной подготовкой донорской раны с одной стороны и неверным выбором способа пластического закрытия дефекта с другой [6]. В настоящий момент реконструктивная хирургия пролежней проекции большого вертела предлагает следующие варианты пластик: первичное ушивание, дермотензия, аутопластика свободным расщепленным кожным трансплантатом, пластика кожно-жировым, кожно-фасциальным и кожно-мышечным лоскутом [7]. Из всех имеющихся методов оптимального, из-за риска специфических осложнений и высокого риска рецидивов, по мнению многих авторов, не существует, поэтому «золотой стандарт» остается предметом поиска [8].
Первичное ушивание: данный метод основан на прямом выдвижении краев раны после иссечения язвенного дефекта с последующим его ушивани ем. Применение данного метода резко ограничено в связи с близким расположением послеоперационного рубца к зоне первичного давления, что ведет к неизбежному рецидиву. Кроме того, основными условиями для данного вида пластики является от сутствие остеомиелита вертела бедренной кости и натяжения тканей в данной области [9]. Дозированное тканевое растяжение (ДТР) решает вышеуказанную проблему благодаря увеличению размеров лоскута, используемого для закрытия дефекта.
Достигается это путем дозированного растяжения покровных тканей посредством спицевого воздействия, которое осуществляется последовательным проведением спиц Киршнера под кожу с постепенным стягиванием краев раневого дефекта (рис. 2, а), баллонной дилатации – расширение кожи с помощью баллонного тканевого расширителя, который вводится в подкожный карман в непосредственной близости к пролежню, с медленным его наполнением воздухом или асептическим раствором, дермотензии с помощью специальной вытяжной повязки, предложенной Johnson в 1993 г. Несмотря на относительную техническую простоту, используется данный метод крайне редко и связано это с длительным периодом заживления раневого дефекта, высокой вероятностью местных осложнений из-за негативного воздействия тракции на раневой процесс с формированием выраженно го рубца в зоне ушивания, что увеличивает риск рецидива [10].
Аутопластика свободным расщепленным кожным трансплантатом (АДТ) – метод выбора в хирургии пролежней проекции тазобедренной области у соматически тяжелых пациентов, который может быть выполнен как окончательный, либо как предварительный этап лечения данной когорты пациентов в зависимости от динамики их состояния.
Особенностью данного метода является его малая травматичность и возможность забора трансплантата необходимой площади, позволяющего ликвидировать обширные декубитальные язвы и тем самым обезопасить пациента от распространения хирургической инфекции с одной стороны и нивелировать белковые и электролитные потери с другой.
Вместе с тем, применение данного метода резко ограничивает состояние трофики лоскута и реципиентной раны, что в большинстве случаев приводит к лизису забранного трансплантата. При положительном же исходе и полном приживлении последнего формируется лишь тонкий слой по кровной ткани с нежным рубцом, который крайне неустойчив к трениям, что часто ведет к смещению трансплантата и рецидиву пролежня (рис. 2, г–е) [10, 11]. Кожно-жировые лоскуты (КЖЛ) довольно широко применяются в реконструкции пролежней проекции большого вертела бедренной кости. Основным их преимуществом является формирование полнослойного покрова в проекции язвенного дефекта с хорошо кровоснабжаемыми тканями. Более того, операция с использованием локального КЖЛ проще и быстрее в техническом исполнении, что важно у соматически тяжелых пациентов.
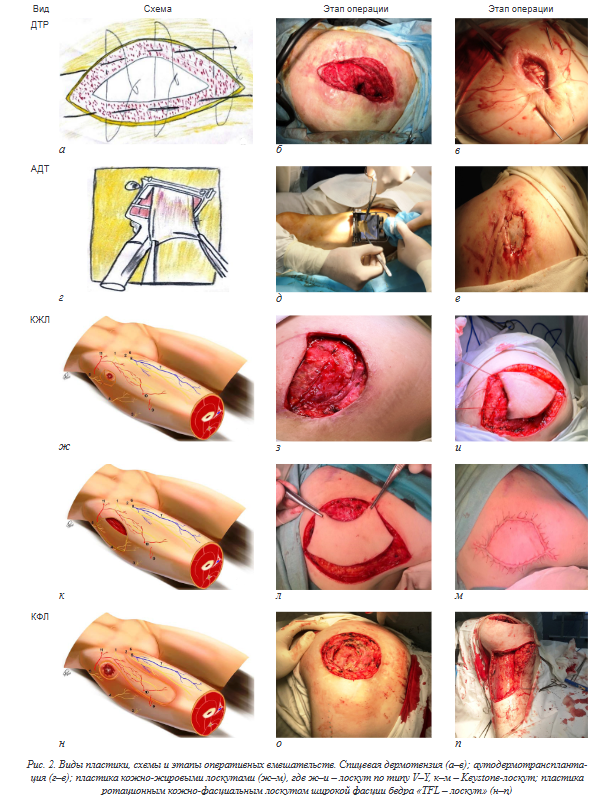
Однако локальные лоскуты гораздо сложнее спроектировать в соответствии с необходимой площадью и геометрией язвенного дефекта, а малоподвижность их основания и чрезмерное натяжение приводит к смещению оси питающего сосуда, с последующей ишемией лоскута и его полным или частичным некрозом [12]. Основными вариантами кожно-жировых лоскутов, которые возможны при закрытии пролежня проекции большого вертела, являются пластика по Keystone, классический вариант кото рой начинается с окаймляющего трапециевидного разреза в виде арки изогнутым основанием к раневому дефекту и выпуклым к его противоположному краю, формируя при этом островковый лоскут с широким жировым основанием и питающими его перфорантными сосудами, который распределяется на всю площадь пролежня узловыми швами (рис. 2, к–м) [13]; островковый кожно-жировой лоскут по типу V–Y, отличается от предыдущей пластики тем, что изначально формируется много угольник, при этом количество углов может варьировать от 3 до 5 в зависимости от конфигурации раневого дефекта, с последовательным пересечением кожи и подкожно-жировой клетчатки и смещением лоскута к пролежневому дефекту (рис. 2, ж–и) [9].
Кожно-фасциальные лоскуты (КФЛ) практически лишены недостатка излишнего натяжения, так как их кровоснабжение осуществляется из сравнительно крупных артериальных перфорантов. По этому именно эти лоскуты являются методом выбора для закрытия пролежней проекции большого вертела. Среди таковых в хирургический обиход вошли лоскуты передней боковой поверхности бедра (ALT-лоскут), лоскут на основе широкой фасции бедра (TFL-лоскут) и его модификации.
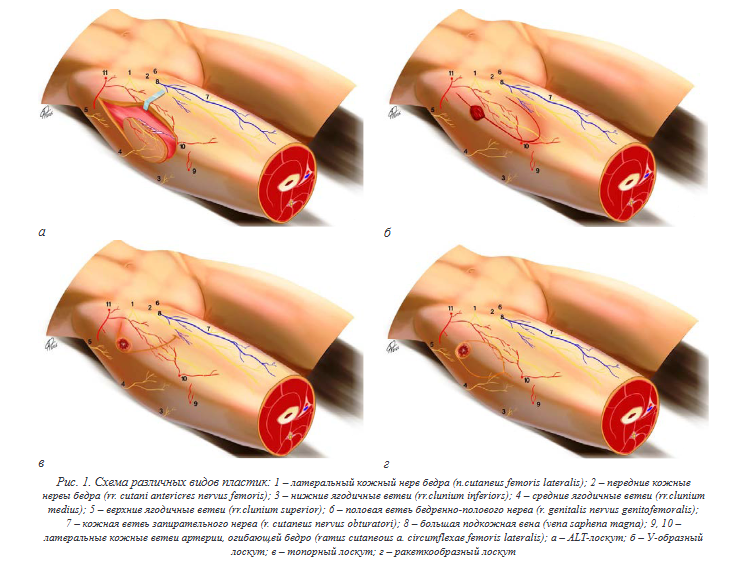
Хирургическая техника ALT-лоскута начинается с формирования линейного разреза от передней верхней ости подвздошной кости до латерального края коленной чашечки, при этом сосудистые перфоранты, как правило, располагаются в пределах средней точки этой линии. После обнаружения всех интересующих перфорантов данной зоны визуали зируется самый дистальный из них, необходимый для мобилизации максимально длинной сосудистой ножки, позволяющей увеличить дугу вращения лоскута. Формирование последнего осуществляется вокруг питающего сосуда посредством иссечения необходимой площади кожи с подлежащей к ней клетчаткой на ранее выделенной сосудистой ножке, которую укладывают в созданную борозду в латеральной широкой мышцы бедра. Медиальный край лоскута рассекается через глубокую фасцию над прямой мышцей бедра до апоневротической перегородки между прямой и латеральной широкой мышцами бедра с ее последующим проксимальным пересечением и обнаружением нисходящей ветви латеральной артерии, огибающей бедренную кость [14]. Затем лоскут переносится в декубитальный дефект проекции большого вертела либо через подкожный туннель на боковой поверхности бедра, либо через открытую борозду, созданную путем разделения кожного мостика между дефектом и лоскутом (рис. 1, а). При выделении лоскута существует высокий риск пересечения латеральной артерии, огибающей бедренную кость, приводящий к некрозу всей кожно-фасциальной основы с потерей альтернативы закрытия дефекта, что резко ограничивает данный метод в широком его применении [15].
TFL-лоскут. Оперативное пособие при использовании данного метода осуществляется в положении пациента на боку, лоскут при этом формируется в зависимости от размеров пролежневого дефекта, предпочтительно до проксимальной трети бедра, где перфузия тканей более надежна. Рассечение лоскута начинается с дистальной его части, с определением сосудистой ножки, и отделением ее единым кожно-фасциальным блоком по направлению снизу-вверх, затем пересекается кожная перемычка между участками донорской и реципиентной раны, что предотвращает сужение лоскута, позволяет ро тировать и продвигать его к пролежневому дефекту (рис. 2, н–п) [16]. Данный вид пластики по сей день считается золотым стандартом в лечении пролежней проекции большого вертела, поскольку имеет хорошее кровоснабжение основания, довольно легко приживается, является легко воспроизводимым, безопасным и надежным методом. Вместе с тем, ряд авторов отмечают, что его первоначальная конструкция имеет такие недостатки, как неудовлетворительное кровоснабжение дистальной части лоскута, который помещается в ложе декубитальной язвы, ротация лоскута приводит к его деформации в виде «собачьего уха», которое является предиктором образования сером и гематом, выраженной деформации донорской зоны [17]. В связи с этим фактом были предложены различные конфигура ции TFL-лоскута: U-образный, топорный, V–Y, ракеткообразный и крыловидный лоскуты. U-образный лоскут широкой фасции в оригинальном своем исполнении простирается от пролежневого дефекта проекции вертела бедренной кости к задней части средней трети бедра и обратно по передневерхней его поверхности. Рассечение лоскута начинается дистально на уровне мышечно-сухожильного соединения, сохраняя при этом подвздошно-большеберцовый тракт снизу, и продолжается в проксимальном направлении в субфасциальной плоскости, затем кожно-фасциальный лоскут сдвигается кзади и фиксируется к донорской ране посредством вертикальных ма трасных швов. Неоспоримыми преимуществами данного метода является: U-образная конструкция лоскута, которая позволяет просто и эффективно его поднять от гребня подвздошной кости, мобилизация проксимальной части увеличивает его объем и упрощает закрытие дефекта вертельной области; изолированное расположение кожного лоскута позволяет избежать разрезов в паховой складке и способствует первичному закрытию донорского участка без «ушей» или точек раздвоения, которые часто приводят к лимфоррее и несостоятельности швов; проксимальное рассечение широкой фасции бедра сохраняет целостность подвздошно большеберцового тракта; траектория рассечения кожно-фасциальных структур позволяет сохранить прилегающий ангиосом для возможного его реконструктивного использования при рецидиве пролежня (рис. 1, б). Вместе с тем, ограниченная площадь и подвижность лоскута зачастую не дает закрыть большие и осложненные пролежни [18].
Топорный лоскут получил свое название из-за разреза в форме топора и во многом решил проблему подвижности лоскута путем увеличения длины разреза в 3–5 раз относительно диаметра дефекта, что позволяет сохранять соотношение между основанием лоскута (расстояния между линией за днего разреза и дефектом) к поперечному разрезу, которая составляет 1:2. Указанная особенность обе спечивает хорошую подвижность тканей за счет комбинированного вращения и перемещения с ми нимальным натяжением (рис. 1, в).
Однако данная модификация имеет право на использование без включения в лоскут фасции, поскольку питающие артерии вокруг ягодичной области находятся глубоко под нижележащими мышцами, как описано Тейлором, а это означает, что ее включение не улучшает кровоснабжение лоскута, а лишь ограничивает его подвижность при мобилизации [9, 19].
Лоскут V–Y на основе широкой фасции бедра в 77 % случаев является успешной методикой, кото рая достигается закрытием пролежневого дефекта наиболее васкуляризованной частью лоскута и позволяет избегать деформации последнего в виде «собачьего уха» (рис. 2, ж–и).
Послеоперационные осложнения, которые в среднем варьируют в диапазоне 20–25 %, в большинстве своем случаев раз решаются консервативными способами, но данная возможность появляется при пролежнях малого и среднего размера, при более обширных дефектах данный вид пластики нецелесообразен из-за излишнего растяжения и сложностей в закрытии донорской раны [20].
Ракеткообразный островковый лоскут – модификация лоскута типа V–Y и его основным преимуществом перед предыдущим является узкая проксимальная часть, благодаря которой широкую дистальную часть лоскута можно легко перенести на место реципиента, а дефект донорской раны в узкой проксимальной части легко закрывается обычным ушиванием (рис. 1, г). Хороша данная модификация при пролежнях малого диаметра [21].
Крыловидный лоскут или лоскут по типу «утиного крыла» – его особенность заключается в транспозиции лоскута к донорской ране формированием треугольного расширения с деэпителизированной частью, что обеспечивает прилегание лоскута к реципиентному ложу, что позволяет ликвидировать остаточную полость и избежать деформации в форме собачьего уха. Минусом данной методики является риск некроза лоскута при пластике крупных декубитальных язв [22].
Каждая из предложенных методик при сохра нении рядя условий имеет право на использование в клинической практике, однако общие их недостатки – ограниченный размер лоскута, из-за которого часто не хватает массива ткани для закрытия большого дефекта, критическое натяжение при пластиках пролежней больших размеров, отсутствие мышечной массы, возникновение мертвого пространства – не возводят их в ранг «идеального метода» в реконструкции декубитальных язв проекции большого вертела.
Поэтому многие клиницисты для пластики данной области прибегают к кожно-мышечным лоскутам (КМЛ), массив которых полностью замещает дефект, образуется мягкая подушка, устойчивая к давлению выше до пустимых 23,7 мм рт. ст. Кроме того, КМЛ являются методом выбора в реконструктивно-пластических операциях, требующих остеотомии, последствия которой нуждаются в хорошо кровоснабжаемой основе, необходимой для приживления лоскута и в качестве такой основы выступают лентовидная, прямая мышцы бедра, а также комбинация из проксимального мышечного сегмента широкой фасции бедра и средней ягодичной мышцы [23].
Вместе с тем, КМЛ считаются технически сложными вмешательствами, требующими тщательного интраоперационного гемостаза и бережного отношения к тканям, необходимости длительного послеоперационного дренирования раневой зоны, проведения антибактериальной терапии как на до операционном этапе, так и после него.
Особого внимания заслуживают методики свободных полнослойных лоскутов с формированием сосудистого микроанастомоза и хирургия, направленная на восстановление иннервации тканей с по мощью формирования анастомоза между чувствительным нервом, располагающимся краниальнее зоны повреждения спинного мозга и нервом используемого лоскута [24].
Однако при использовании указанных методик стоит помнить о высоком риске тромбоза при новосозданном межсосудистом анастомозе, что влечет за собой некроз лоскута. По данным метаанализа P. R. Zwanenburg (2021) восстановление иннервации заметно снижает частоту рецидивов пролежней (с 37 % до 1 %), но из-за травматичности и увеличения площади раневой поверхности отмечается рост осложнений с 19 % до 95 % [25].
Недостатки представленных вариантов реконструктивно-пластических операций являются отправной точкой в поисках «идеальной операции» в современной реконструктивной хирургии пролежней проекции большого вертела бедренной кости, которая могла бы сочетать в себе малую травматичность, сохранять полноценное кровоснабжение лоскута, исключала бы образование мертвых полостей, позволяла закрыть пролежневый дефект без натяжения с ликвидацией остаточной полости. Проспективное клиническое исследование.
В качестве оперативного пособия для закрытия пролежневого дефекта были применены следующие виды пластик:
1) спицевая дермотензия (n=8); 2) пластика свободным расщепленным трансплантатом (n=8); 3) пластика с использованием кожно-жировых (n=8) и кожно-фасциальных (n=23) лоскутов (V–Y, по Keystone, ротационный кожно-фасциальный лоскут широкой фасции бедра).
Хирургическое лечение. 1. Спицевая дермотензия была выполнена 8 пациентам.
Техника операции: после иссечения рубцово измененных краев раны и удаления патологических грануляций из дна раны в 1,5 от края раны через кожу и подкожную клетчатку проводили спицы Киршнера; направление спиц – параллельно краю раны и перпендикулярно вектору натяжения кожи; проводили лигатуры через края раны и установленные в них спицы, после чего лигатуры постепенно натягивали, сближая спицы и края раны до соприкосновения; в полость раны устанавливали проточно-аспирационную дренажную систему (рис. 2, а–в).
2. Пластика свободным расщепленным кожным трансплантатом применена у 8 пациентов.
Техника операции: дисковым дерматомом забирали расщепленный трансплантат толщиной 0,35–0,40 мм с наружной поверхности бедра; трансплантат фиксировали на гранулирующую поверхность пролежневого дефекта, закрывали повязкой (рис. 2, г–е).
3. Пластика ран кожно-жировыми лоскутами проведена 8 пациентам.
Ключевым моментом в оперативном пособии явился отказ от рассечения собственной фасции с целью снижения травматизации тканей и снижения риска пересечения перфорантных сосудов и нервов. Виды применяемых пластик: пластика по Keystone выполнена 5 пациентам (рис. 2, к–м), пластика островковым кожно-жировым лоскутом по типу V–Y пластики – 3 больным (рис. 2, ж–и).
4. У 37 (60 %) пациентов пластика проводилась с помощью ротационного кожно-фасциального лоскута широкой фасции бедра (TFL – лоскут) (рис. 2, н–п). Для каждого из представленных видов пластик оценивали частоту ранних осложнений в течение 2 недель от выполненной операции, а также частоту рецидивов, возникших в течение 3 месяцев после каждого из видов примененных операций.
Статистический анализ данных. Статистическая обработка полученных данных выполнена при помощи пакета прикладных программ IBM SPSS Statistics 20. Проверку нормальности распределения количественных признаков проводили с использованием критерия Шапиро–Уилка.
Все исследованные показатели не имели нормального распределения, поэтому оценку статистической значимости различий при сравнении групп по количественным признакам выполняли непараметрическими методами.
Для сравнения качественных показателей в группах использовали Хи-квадрат Пирсона. n – объем анализируемой подгруппы, р – величина статистической значимости различий.
Критическое значение уровня значимости принимали равным 5 % (р≤0,05). При использовании множественных сравнений уровень значимости различий указан в виде скорректированного значения padjusted.
Результаты.
При анализе полученных результатов было зафиксировано 21 (34 %) осложнение из 61 выполненных операций. Чаще всего развивались частичная или полная несостоятельность швов, раневая инфекция, ишемия лоскута, лимфоррея. В группе пациентов со спицевой дермотензией в 4 случаях из 8 имелись признаки ишемии, которая привела к частичному некрозу лоскута и прорезыванию швов. Пластика расщепленным кожным трансплантатом у 4 из 8 пациентов осложнилась раневой инфекцией с полным лизисом трансплантата.
Оперативное лечение кожно-жировыми лоскутами (n=8) осложнилось в 3 случаях в виде несостоятельности швов, которые носили частичный характер, при этом методика Keystoneлоскута (n=5) имела 1 осложнение в виде частичной несостоятельности швов, островковый лоскут по типу V–Y (n=3) имел 2 осложнения, также связанных с частичной несостоятельностью швов.
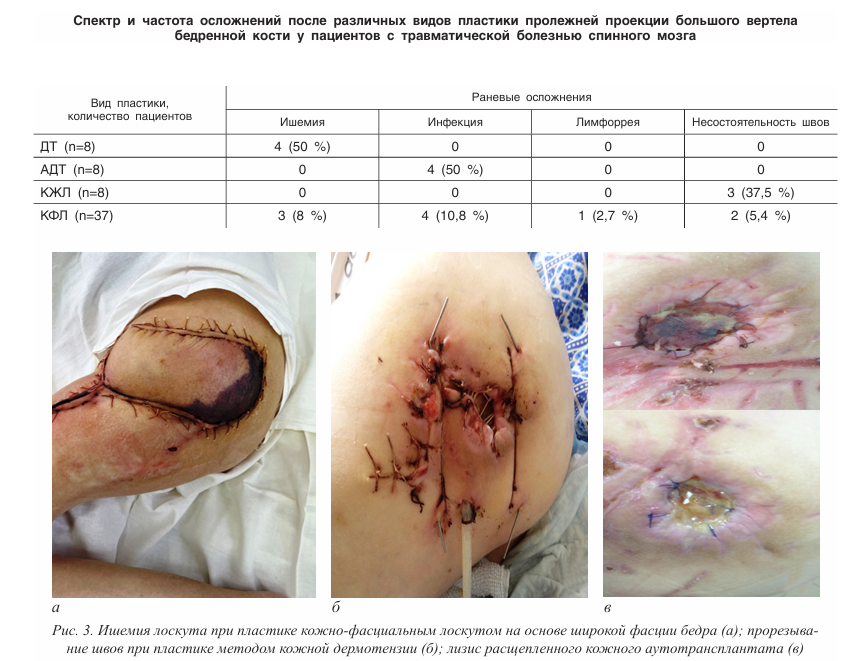
При применении TFL-лоскута осложнения в раннем послеоперационном периоде развились в 10 случаях из 37, среди которых превалировали: раневая инфекция – 4, ишемия лоскута – 3, несостоятельность швов – 2, выраженная лимфоррея – 1 (таблица). Таким образом, частота осложнений в раннем послеоперационном периоде составила 34 % от общего количества выполненных пластик, при этом из них: 50 % после спицевой дермотензии, 50 % после аутодермотрансплантации, 37,5 % после использования кожно-жировых лоскутов, 27 % после применения кожно-фасциальных лоскутов (Хи-квадрат Пирсона 0,055, padjusted 0,050). Рецидивы пролежней после пластики методом дермотензии развились у 4 пациентов (50 %); свободная кожная пластика расщепленным кожным трансплантатом сопровождалась рецидивами в 5 случаях из 8: в 4 случаях в раннем послеоперационном периоде из-за присоединения инфекции и лизиса кожного трансплантата и в 1 случае в отдаленном послеоперационном периоде за счет пролежня уже прижившегося трансплантата (62,5 %). У пациентов, оперированных с использованием кожно-жировых лоскутов, рецидивы не наблюдались. У пациентов с кожно-фасциальными лоскутами рецидивы в течение 3-х месяцев после операции зафиксированы у 2 пациентов из 37 (5,4 %) (рис. 3). Успешная пластика пролежней проекции большого вертела без осложнений и рецидивов зафиксирована в 40 (66 %) случаях из 61: после выполнения спицевой дермотензии – у 4 пациентов из 8; после выполнения аутопластики расщепленным кожным трансплантатом – у 4 пациентов из 8; после использования кожно-жировых местных лоскутов – у 5 пациентов из 8; после закрытия пролежня TFLлоскутом – у 27 пациентов из 37 (рис. 4).
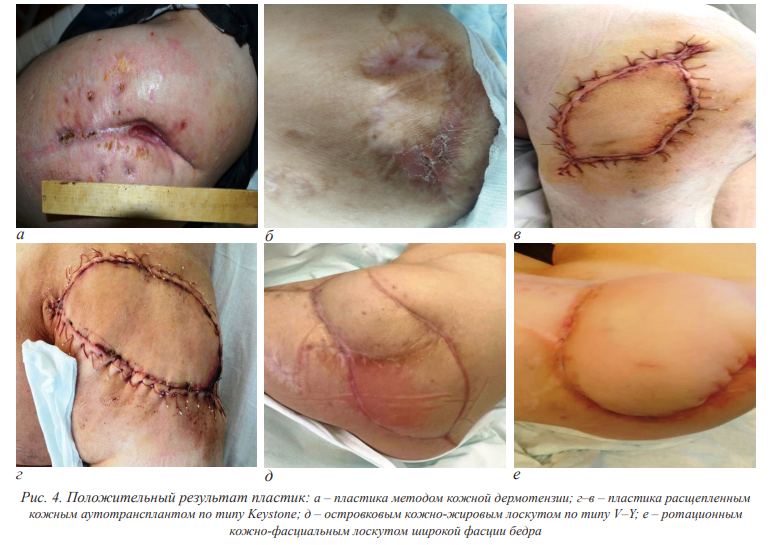
Обсуждение.
Проблема выбора метода пластики декубитальных язв проекции большого вертела бедренной кости у пациентов с повреждением спинного мозга является актуальным вопросом в современной реконструктивно-пластической хирургии. Хроническая инфекция, денервация тканей, истощение местных регенераторных ресурсов определяют исход реконструктивной операции. Пластика свободными расщепленными трансплантатами, видимо, в наименьшей степени соответствует требованиям к реконструктивно-пластическим вмешательствам на пролежнях тазобедренной области из-за высокого риска инфекционного лизиса трансплантата и высокой вероятности развития рецидива. Задачу предупреждения ранних инфекционных осложнений после аутодермотрансплантации отчасти можно решить за счет использования современных перевязочных материалов, применения бактериофагов [26]. Но проблема низкого качества восстановленных кожных покровов и высокой вероятности рецидива после пластики пролежня расщепленным трансплантатом остается острой. Аппликация жировой ткани в дно хронической раны перед пересадкой расщепленного кожного трансплантата, возможно, способна ее решить [27].
Однако пока данных об эффективности этой методики в отношении пролежней нет. Полученные результаты в отношении количества и вида осложнений, полученных в ходе выполненной работы, в целом соответствует мировому и отечественному опыту в реконструктивной хирургии пролежней [28]. Надо отметить, что к рецидивам были склонны пациенты, у которых в раннем послеоперационном периоде наблюдались нарушения кровообращения и раневая инфекция в донорских лоскутах и трансплантатах.
Отдельно нужно указать, что в исследование не включены пациенты с пролежнями, в лечении которых применялась пластика перемещенными кожно-мышечными лоскутами. Эта методика имеет некоторые преимущества [29]. Кожно-мышечные лоскуты обеспечивают максимально возможную по объему, хорошо кровоснабжаемую мягкотканную основу в реципиентной ране, что сокращает риски рецидивов пролежня [30]. Вместе с тем мобилизация кожно-мышечного лоскута приводит к формированию обширной, глубокой донорской раневой поверхности.
Послеоперационный период сопряжен с риском образования гематом и их инфицирования, что требует тщательного интраоперационного гемостаза с одной стороны и длительного послеоперационного дренирования с другой [31].
Заключение.
Наименее эффективными и наиболее рискованными с точки зрения развития ишемических и инфекционных осложнений методами хирургического лечения пролежней проекции большого вертела бедренной кости у пациентов с ТБСМ являются дермотензия и аутодермопластика расщепленным трансплантатом. При этом применение аутодермотрансплантации возможно и целесообразно в ограниченной группе пациентов, которым противопоказаны травматичные вмешательства, для решения ограниченных задач – максимально быстрого и минимально травматичного сокращения площади раневой поверхности. Наиболее функциональными пластиками пролежней проекции большого вертела являются методики с использованием местных кожно-жировых лоскутов или TFL-лоскута на основе широкой фасции бедра.
При этом остается открытым вопрос нивелирования недостатков, присутствующих в оперативном пособии предложенных методик (недостаточное кровоснабжение дистальной части TFL-лоскута, недостаточность пластического материала при закрытии больших по площади раневых поверхностей, сохранение мертвого пространства в тканях с продукцией сером, высокий уровень натяжения тканей при использовании КЖЛ), которые во многом определяют исход первичного оперативного лечения, повышают процент рецидивов. В связи с этим фактом современная реконструктивно-пластическая хирургия пролежней проекции большого вертела бедренной кости требует новых фундаментальных и практических знаний, позволивших бы снизить частоту осложнений и рецидивов.
Литература
1. Chen G., Wang T., Zhong L. et al. Telemedicine for Preventing and Treating Pressure Injury After Spinal Cord Injury: Systematic Review and Meta-analysis. J Med Internet Res. 2022. Vol. 24, № 9. P. 37618.
2. Marfil-Gómez R. M., García-Mayor S., Morales-Asencio J. M. et al. Pressure levels in the trochanter area according to repositioning at different degrees of inclination in healthy subjects. J Tissue Viability. 2020. Vol. 29, № 2. P. 125–129.
3. Labeau S. O., Afonso E., Benbenishty J. et al. Prevalence, associated factors and outcomes of pressure injuries in adult intensive care unit patients: the DecubICUs study. Intensive Care Med. 2021. Vol. 47, № 2. P. 160–169.
4. Fagotti de Almeida C. E., Cirino Dos Santos A. P. B., Biaziolo C. F. B. et al. The role of the perioperative prone position in the low recurrence of pressure injuries in the pelvic region. J Wound Care. 2022. Vol. 31, № 1. P. 92–98.
5. Fähndrich C., Gemperli A., Baumberger M. et al. Treatment approaches of stage III and IV pressure injury in people with spinal cord injury: A scoping review. J Spinal Cord Med. 2023. Vol. 46, № 5. P. 705–715.
6. Labeau S. O., Afonso E., Benbenishty J. et al. Prevalence, associated factors and outcomes of pressure injuries in adult intensive care unit patients: the DecubICUs study. Intensive Care Med. 2021. Vol. 47, № 2. P. 160–169.
7. Zhao Z., Zhang B., Liu Y. et al. Repair of bedsore over greater trochanter in paraplegic patients with rectus femoris island myocutaneous flap. Zhonghua Shao Shang Za Zhi. 2021. Vol. 30, № 3. P. 227–30.
8. Thomson C. H., Choudry M., White C. et al. Multi-disciplinary management of complex pressure sore reconstruction: 5-year review of experience in a spinal injuries centre. Ann R Coll Surg Engl. 2017. Vol. 99, № 2. P. 169–174.
9. Jósvay J., Klauber A., Both B. et al. The operative treatment of pressure sores in the pelvic region: A 10-year period overview. J Spinal Cord Med. 2015. Vol. 38, № 4. P. 432–8.
10. Norman G., Wong J. K., Amin K. et al. Reconstructive surgery for treating pressure ulcers. Cochrane Database Syst Rev. 2022. Vol. 10, № 10. P. CD012032.
11. Бесчастнов В. В., Антошина В. В., Орлинская Н. Ю. и др. Микротрансплантация кожи ускоряет заживление ран за счет усиления процессов пролиферации и васкуляризации. Новости хирургии. 2023. Т. 31, № 3. С. 190–202. .
12. Османов Э. Г., Шулутко А. М., Слепнев С. Ю. и др. Актуальные вопросы хирургической коррекции декубитальных язв (обзор). Московский хирургический журнал. 2021. № 2. С. 77–86.
13. Аникин А. И., Деденков О. А., Васильков Д. В. и др. Опыт лечения плантарных раневых и язвенных дефектов. Раны и раневые инфекции. Журнал имени проф. Б. М. Костюченка. 2020. Т. 6, № 3. С. 30–33.
14. Hifny M. A. The pedicled anterolateral thigh flap for trochanteric pressure sore reconstruction: Technical notes to optimize surgical outcomes. Arch Plast Surg. 2021. Vol. 48, № 1. P. 114–120.
15. Lauer H., Goertz O., Landscheidt K., Hernekamp J. F. Die proximal gestielte Anterior-lateral-thigh-Lappenplastik zur Rekonstruktion komplexer Weichteilwunden der Hüft- und kaudalen Rumpfregion [The proximally pedicled anterolateral thigh flap for reconstruction of complex soft tissue wounds of the hip and caudal trunk region]. Chirurg. 2022. Vol. 93, № 4. P. 388–394. German.
16. Singh R., Wadhwani J., Rohilla R. K., Kaur K. Proximal femoral resection and Tensor Fascia Lata flap for recalcitrant trochanteric pressure ulcers. Spinal Cord Ser Cases. 2019. Vol. 5. P. 15.
17. Lakhiani C., DeFazio M. V., Han K. et al. Donor-Site Morbidity Following Free Tissue Harvest from the Thigh: A Systematic Review and Pooled Analysis of Complications. J Reconstr Microsurg. 2020. Vol. 32, № 5. P. 342–57.
18. DeFazio M. V., Economides J. M., Felder J. M. 3rd, Attinger C. E. The U-Shaped Tensor Fasciae Latae Musculocutaneous Flap for Coverage of Trochanteric Defects: Simplified Design to Minimize Donor-Site Morbidity. Plast Reconstr Surg. 2015. Vol. 136, № 2. P. 288e–290e.
19. Demirseren M. E., Gökrem S., Ozdemir O. M. et al. Hatchet-shaped tensor fascia lata musculocutaneous flap for the coverage of trochanteric pressure sores: a new modification. Ann Plast Surg. 2003. Vol. 51, № 4. P. 419–22.
20. Siddiqui A., Wiedrich T., Lewis Jr V. L. Tensor Fascia Lata V—Y Retroposition Myocutaneous Flap: Clinical Experience. Annals of plastic surgery. 1993. Vol. 31, № 4. P. 313–317.
21. Yu G., Pang S., Li G. The tensor fascia lata racket shape myocutaneous island flap. Zhonghua Zheng Xing Wai Ke Za Zhi. 2001. Vol. 17, № 5. P. 261–3.
22. Aslan G., Tuncali D., Bingul F. et al. The “duck” modification of the tensor fascia lata flap. Ann Plast Surg. 2005. Vol. 54, № 6. P. 637–9. https:// doi.org/10.1097/01.sap.0000162519.25430.1a.
23. Ryoo H. J., Park J. H., Kim D. Y. Vastus Lateralis and Vastus Intermedius Myocutaneous Flap Reconstruction for Complicated Trochanteric and Ischial Pressure Sores with Extended Girdlestone Resection: A Case Series. Orthop Surg. 2023. Vol. 15, № 10. P. 2612–2620.
24. Мирзаева Л. М. Предикторы осложнений и летальных исходов травматических повреждений спинного мозга. Кубанский научный медицинский вестник. 2020. Т. 27, № 1. С. 59–71.
25. Zwanenburg P. R. Systematic review and meta-analysis of sensate versus non-sensate flaps for the prevention of pressure ulcer recurrence among individuals with spinal cord disease. Spinal Cord. 2021. Vol. 59, № 5. P. 463–473.
26. Бесчастнов В. В., Рябков М. Г., Леонтьев А. Е. и др. Исследование in vitro жизнеспособности бактериофагов в составе гидрогеля. Современные технологии в медицине. 2021. Т. 13, № 2. С. 32–39.
27. Рябков М. Г., Спиридонов А. А., Бесчастнов В. В. и др. Лечение хронических ран комбинацией аутодермопластики и липотрансфера. Клиническая и экспериментальная хирургия. Журнал имени академика Б. В. Петровского. 2018. Т. 6, № 4. С. 17–23
28. Irmak F. Management and Treatment of Pressure Ulcers: Clinical Experience. Sisli Etfal Hastan Tip Bul. 2019. Vol. 53, № 1. P. 37–41.
29. Huiming G. Study on the characteristics of microcirculation in the site of pressure ulcer in patients with spinal cord injury. Sci Prog. 2021. Vol. 104, № 3. P. 368–404.
30. Sun J. L. Clinical effects of superior gluteal artery perforator “buddy flap” in repairing pressure ulcer in sacrococcygeal region. Zhonghua Shao Shang Za Zhi. 2020. Vol. 36, № 8. P. 726–729.
31. Sinnott C. J. Dual-Plane Gluteal Myocutaneous Flap for Reconstruction of Ischial Tuberosity Pressure Wounds. Annals of plastic surgery. 2020. Vol. 85, №1. P. 23–S2
Автор:
М. С. Балеев Городская клиническая больница № 7 Ленинского района г. Нижнего Новгорода имени Е. Л. Березова 603011, Россия, г. Нижний Новгород, ул. Октябрьской революции, д. 66а
Теги: пролежни
234567 Начало активности (дата): 12.05.2026
234567 Кем создан (ID): 989
234567 Ключевые слова: пролежни, осложнения, травма спинного мозга, травматическая болезнь спинного мозга, лечение ран, пластика ран
12354567899
Похожие статьи
Пролежни при переломе шейки бедра.Рентген на дому 8 495 22 555 6 8
Бедренная кость
Хирургическая тактика в лечении юношеского эпифизеолиза головки бедренной кости
Приспособительные стереотипы опорных реакций стоп у больных с коксартрозом после эндопротезирования тазобедренного сустава



